Sabemos que a análise ecocardiográfica através do strain é uma importante ferramenta na estratificação dos pacientes com doença arterial coronariana (DAC) crônica, podendo identificar alterações de forma muito precoce e possibilitando, assim, o emprego de intervenções (medicamentosas ou invasivas) com o objetivo de redução de desfechos e melhora de sobrevida.
A área mais suscetível a isquemia está localizada na região subendocárdica e, nessa localidade, as fibras estão orientadas no sentido longitudinal, portanto a avaliação da deformação longitudinal pelo strain é um excelente marcador para a presença de isquemia em comparação com a ecocardiografia convencional.
Alterações das medidas regionais do strain pelo speckle tracking, gerando heterogeneidade de ativação miocárdica (alteração na sequência temporal de encurtamento e alongamento do miocárdio) são indicadores de isquemia.
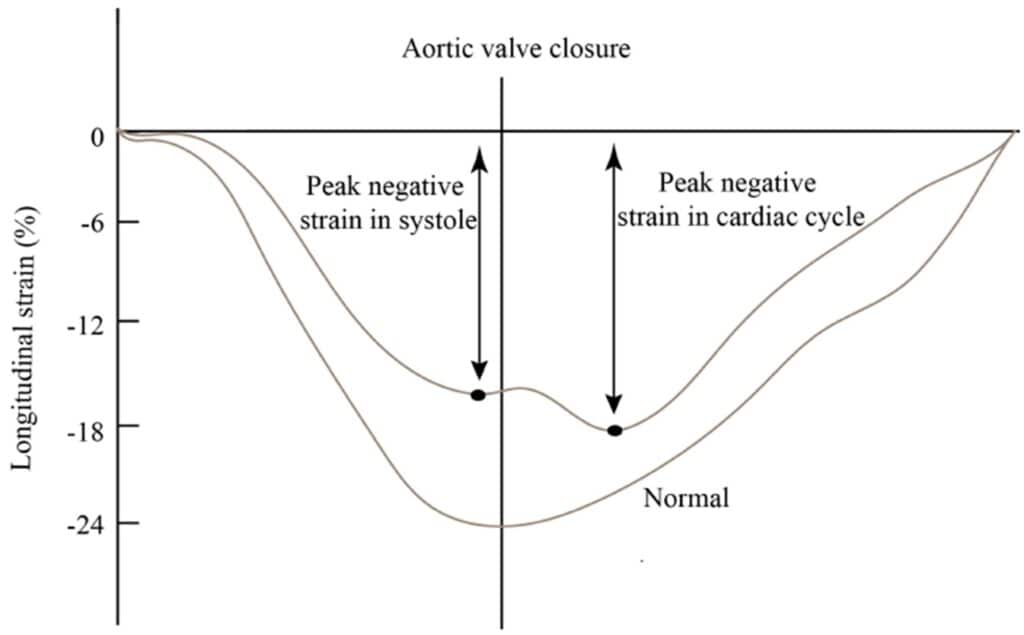
Contudo, não somente a amplitude do encurtamento é reduzida, como também o início e a duração da contração das fibras são alterados, o que gera um encurtamento ou espessamento característico do miocárdio após o fechamento da valva aórtica.
Essa alteração é chamada de contração (encurtamento) pós-sistólica e é característica do desenvolvimento de isquemia, apesar de também poder correr em outras condições que cursem com disfunção regional, como fibrose e dissincronia.
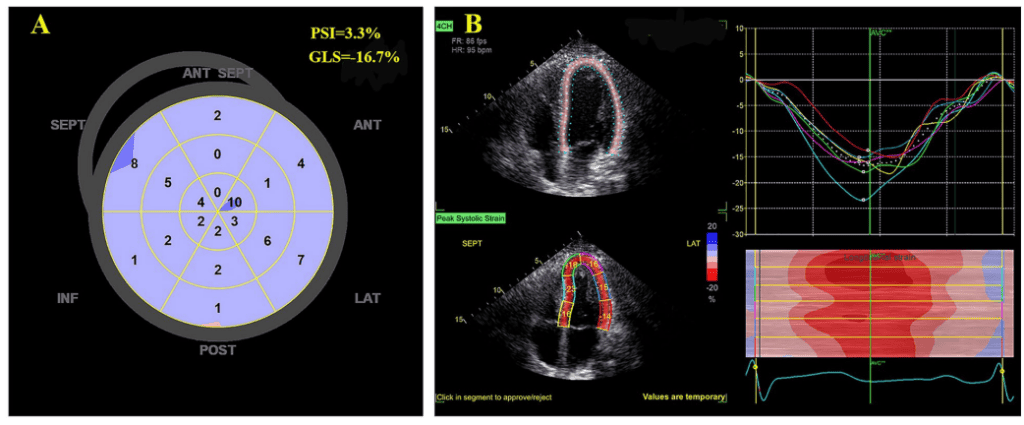

Podemos entender, portanto, que a contração pós-sistólica funciona como um atraso do relaxamento para que a região isquêmica possa encurtar, enquanto a pressão do ventrículo esquerdo (VE) reduz e o tecido circundante relaxa.
A forma mais comumente utilizada para quantificar a contração (encurtamento) pós-sistólica é através do cálculo do índice de contração pós-sistólica (PSI – post- systolic index):
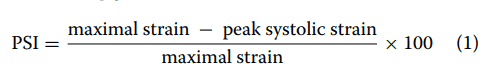
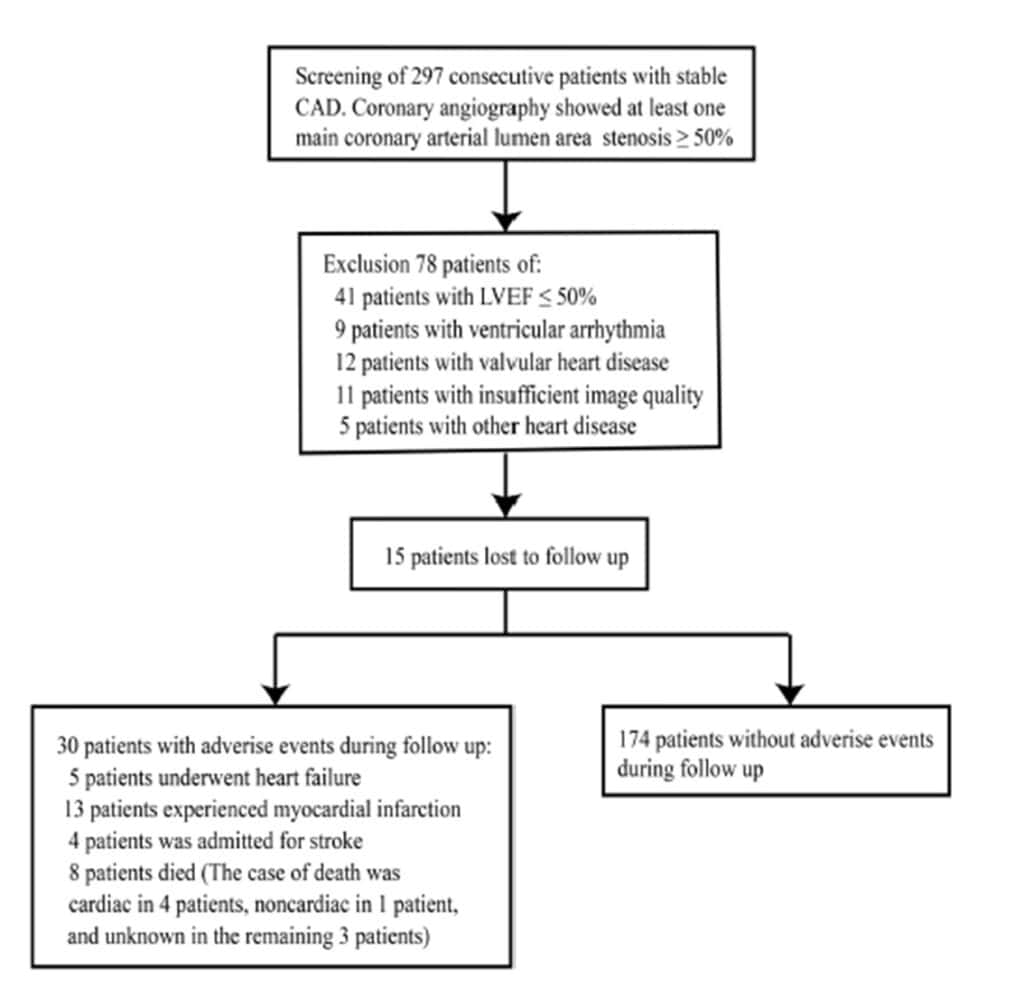
Um estudo prospectivo analisou 297 pacientes com diagnóstico clínico de DAC estável entre o período de abril de 2016 e dezembro de 2020.

Os critérios de exclusão foram: (1) lesão < 50% na cinecoronariografia, (2) fração de ejeção do VE ≤50%, (3) sinais de insuficiência cardíaca ou síndrome coronariana aguda nos últimos 12 meses, (4) outras doenças cardíacas e (5) imagens ecocardiográficas subótimas. Um total de 204 pacientes foram incluídos no estudo.
O índice de contração pós-sistólica foi obtido pela média dos 18 segmentos miocárdicos. A presença de contração pós-sistólica foi definida como um PSI > 20% em pelo menos um segmento miocárdico.
Todos os pacientes foram submetidos a estratificação invasiva com cateterismo cardíaco para confirmar a presença de DAC e a presença de estenose ≥50% em pelo menos uma artéria coronária principal foi o critério utilizado para o diagnóstico de DAC.
Os desfechos compostos foram (1) mortalidade por todas as causas, (2) insuficiência cardíaca e (3) infarto miocárdico ou acidente vascular encefálico. Dos pacientes avaliados, 15 perderam seguimento.
Um total de 204 pacientes (idade média 59±10, sendo 73% homens) foram avaliados durante um seguimento médio de 24 meses. Desses, 30 pacientes (14.7%) apresentaram desfecho composto, sendo 5 com insuficiência cardíaca, 13 com infarto agudo do miocárdio, 4 pacientes com acidente vascular encefálico e 8 pacientes foram à óbito (causa cardíaca 4, causa não cardíaca 1, causa desconhecida 3).
Esses pacientes eram mais velhos, com classe funcional (NYHA) entre III-IV e com valores absolutos de strain global longitudinal (SGL) menores (−15.2±3.1% vs. −17.4±2.8%, p<0.05).
Além disso, foi observado um maior índice de contração pós-sistólica (12.8% [IQR, 7.4–15.0%] vs. 6.3% [IQR, 4.4–9.3%], p<0.05) e maior quantidade de segmentos com contração pós-sistólica quando comparado com os pacientes que não apresentaram desfecho composto.
Não houve diferença significativa entre os parâmetros de função diastólica, espessura da parede ventricular, volumes ventriculares e fração de ejeção do VE entre os grupos (p > 0.05).
No total, 99 pacientes (48.5%) apresentaram contração pós-sistólica, sendo 62 (30.4%) com até dois segmentos acometidos e 43 pacientes (21.1%) com ≥3 segmentos acometidos.
Os pacientes com ≥3 segmentos acometidos tiveram pior classe funcional (III-IV) e menor relação E/A (0.7 [IQR, 0.6–0.9] vs. 0.8 [IQR, 0.7–0.9], p<0.05) em relação aos pacientes sem contração pós-sistólica.
Um maior número de paredes com contração pós-sistólica se associou a maior incidência de eventos adversos, uma fração de ejeção do VE menor, volume sistólico do VE maior e menor SGL.
A média do SGL dos pacientes sem contração pós-sistólica foi de −17.7±2.4%, dos com 1-2 paredes acometidas foi de −17.4±2.8% e os com ≥3 paredes com contração pós-sistólica, de −15.2±3.5%.
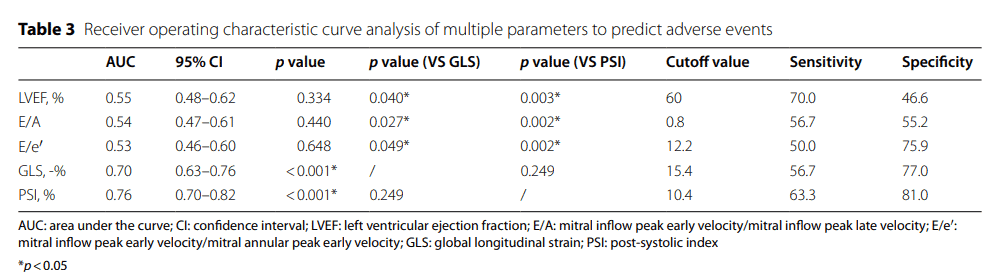
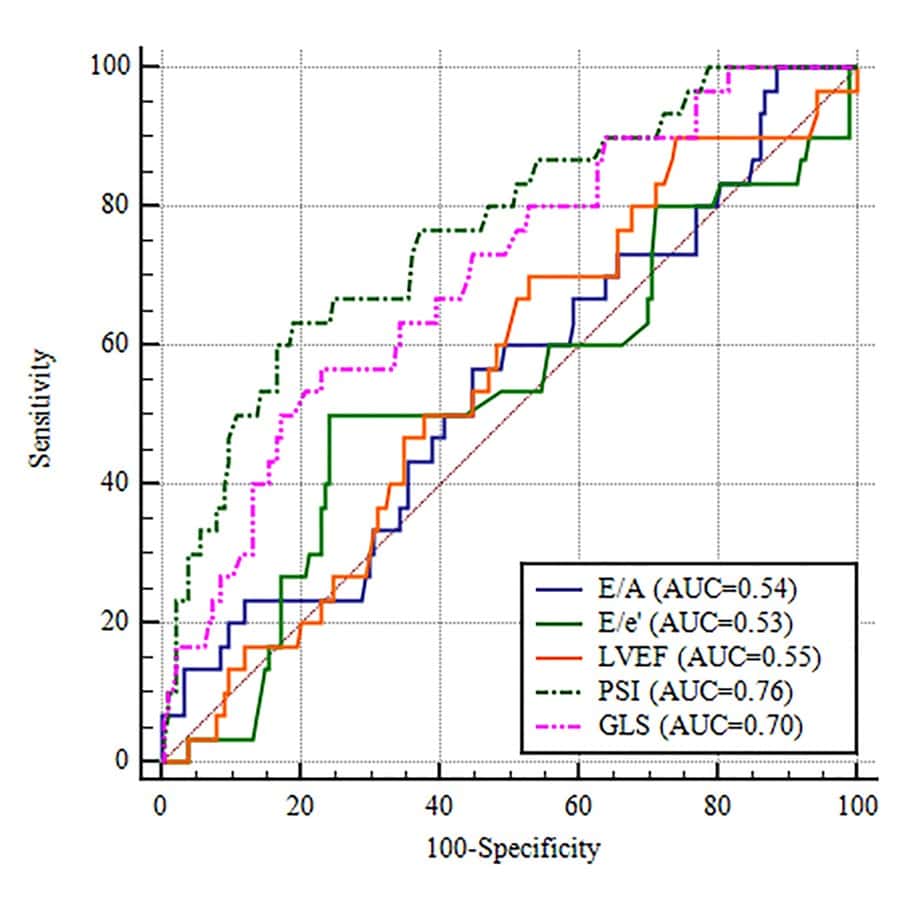
Entre os parâmetros ecocardiográficos avaliados, o índice de contração pós-sistólica foi superior como preditor de risco para eventos adversos (AUC=0.76 [PSI] vs. 0.55 [LVEF], p=0.003; 0.76 [PSI] vs. 0.54 [E/A], p=0.002; 0.76 [PSI] vs. 0.53 [E/e′], p=0.002).
O ponto de corte do PSI foi de 10.4% com sensibilidade de 63.3% e especificidade de 81%. Enquanto que o ponto de corte de -15.4% do SGL teve sensibilidade de 56.7% e especificidade de 77.0%, sem haver diferença significativa entre esses dois parâmetros (AUC=0.76 [PSI] vs. 0.70 [GLS], p=0.249).
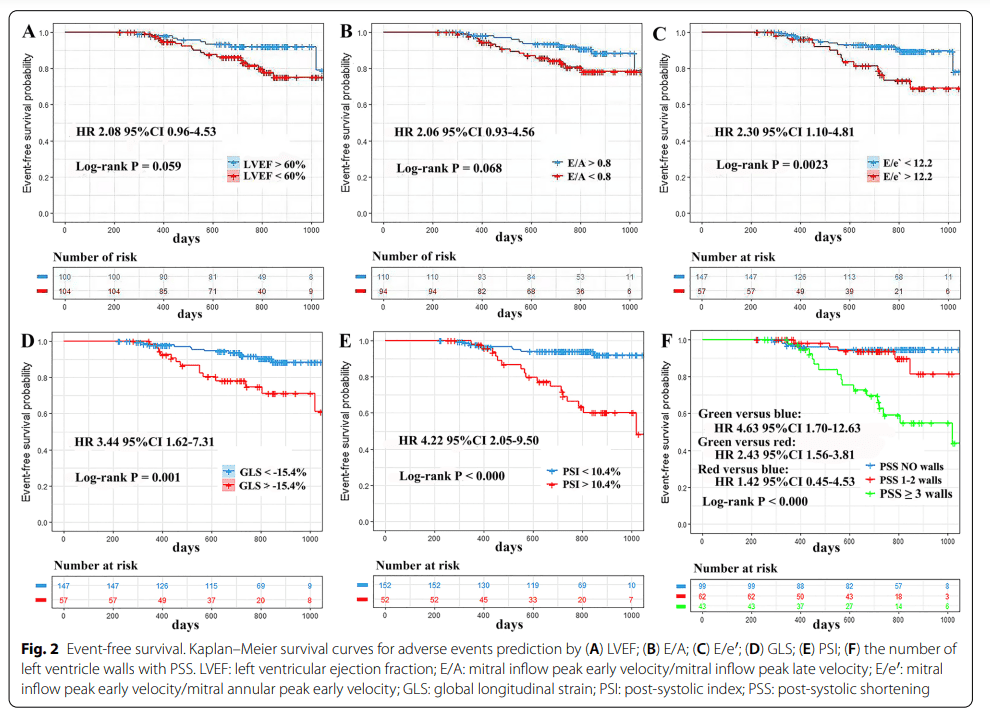
Todos os parâmetros avançados (SGL, PSI e número de paredes com contração pós-sistólica) apresentaram diferença significativa em relação à sobrevida (p<0.05), enquanto que os parâmetros convencionais (fração de ejeção do VE, relação E/A), com exceção da relação E/e´, não apresentaram diferença significativa.
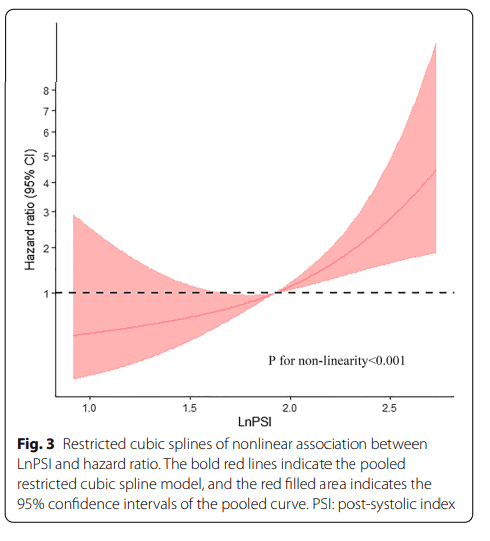
Idade (HR 1.06, 95%CI 1.01–1.10, p=0.008), hipertensão arterial (HR 2.38, 95%CI 1.01–5.59, p=0.046), classe funcional III-IV (HR 2.24, 95%CI 1.05–4.76, p=0.036), SGL (HR 0.85, 95%CI 0.76–0.95, p=0.004) e PSI (HR 1.19, 95%CI 1.09–1.29, p=0.001) se associaram de forma significativa à eventos adversos.
Destes, apenas o número de paredes acometidas e o PSI foram considerados, de forma independente, como preditores significantes .
Ainda, foi realizado uma análise do impacto da presença de contração pós-sistólica em pacientes com SGL > 15.4% em que foi observado um valor prognóstico superior do PSI comparado com o SGL (AUC=0.73[PSI] vs. 0.58[GLS], p=0.024). Portanto, em pacientes com GLS normal ou levemente reduzido, o PSI é melhor parâmetro prognóstico.
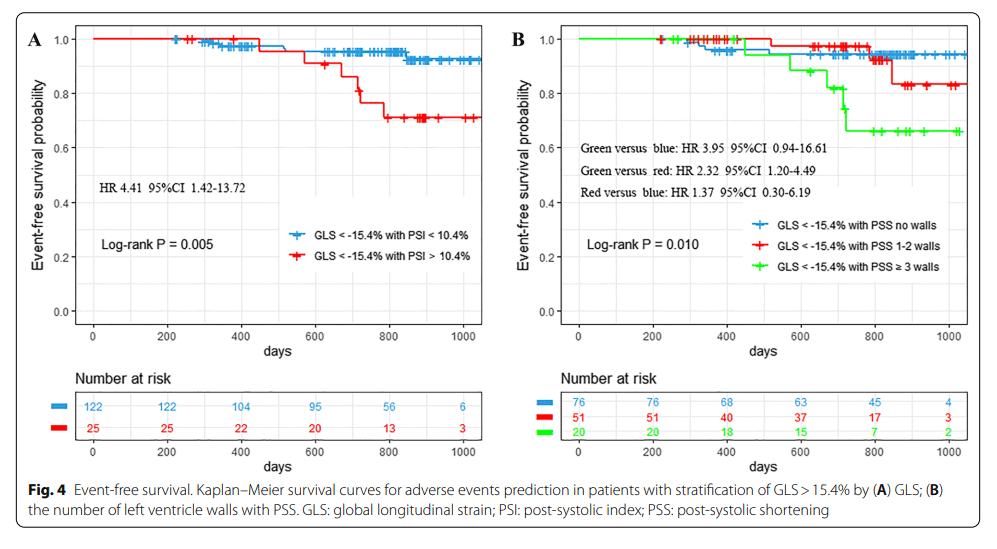
O estudo conclui, desta forma, que o PSS e o número de paredes acometidas apresentam, de forma consistente, valor prognóstico em predizer eventos adversos, sendo a presença de contração pós-sistólica possivelmente superior ao valor do SGL em pacientes com SGL normal ou levemente reduzido.
Graduado em medicina pela Universidade Potiguar (UnP). Possui residência em Clínica Médica pelo Hospital Universitário Onofre Lopes – HUOL (UFRN) e em Cardiologia pelo Procape – UPE. Porta o título de especialista em Cardiologia pela Sociedade Brasileira de Cardiologia (SBC) e é pós-graduado em Ecocardiografia, pela ECOPE.