Finalizando a série sobre próteses cardíacas, vamos falar um pouco sobre os padrões patológicos na avaliação ecocardiográfica dos fluxos e das estruturas das próteses.
Tópicos
Avaliação Hemodinâmica
– Para a análise do fluxo das próteses, tanto para leões estenóticas quanto para as regurgitantes, praticamente usamos os mesmos parâmetros utilizados para as valvas nativas:
1- Área do orifício efetivo das próteses: deve ser estimada pela equação de continuidade. A planimetria não deve ser utilizados para avaliar próteses metálicas; o PHT, embora não seja um método validado para próteses cardíacas, pode ser útil para diferenciar uma prótese mitral normofuncionante de uma estenótica;
2- Gradientes pressóricos: deve-se dar mais valor ao gradiente médio do que ao gradiente máximo, pois as próteses podem ter velocidades instantâneas maiores no momento da abertura valvar, diminuindo rapidamente durante o restante do ciclo cardíaco;
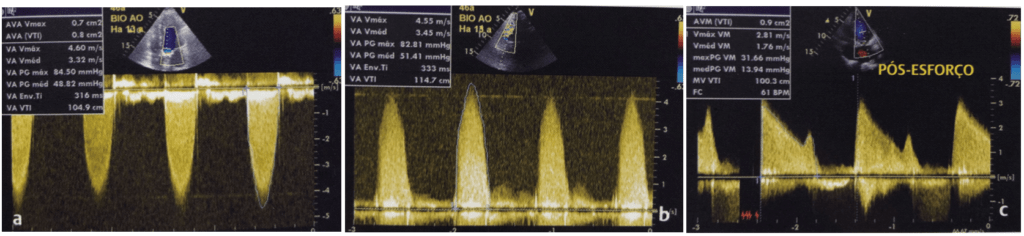
3- Índice de Velocidade do Doppler (IVD): outra forma possível para estimar possíveis estenoses das próteses aórticas é pelo cálculo do índice que correlaciona as velocidades máximas ou a integral das velocidades entre o fluxo subvalvar (VSVE) e a velocidade do fluxo pela prótese –> IVD = VTI vsve / VTI prótese;
4 – Os refluxos patológicos: podem ser quantificados utilizando-se os mesmos critérios empregados nas valvas nativas, sobretudo nas aórticas (origem do refluxo – protético ou paraprotético -, área ocupado pelo jato na VSVE e até onde o jato se estende no VE, além da avaliação da intensidade do sinal pelo Doppler contínuo);
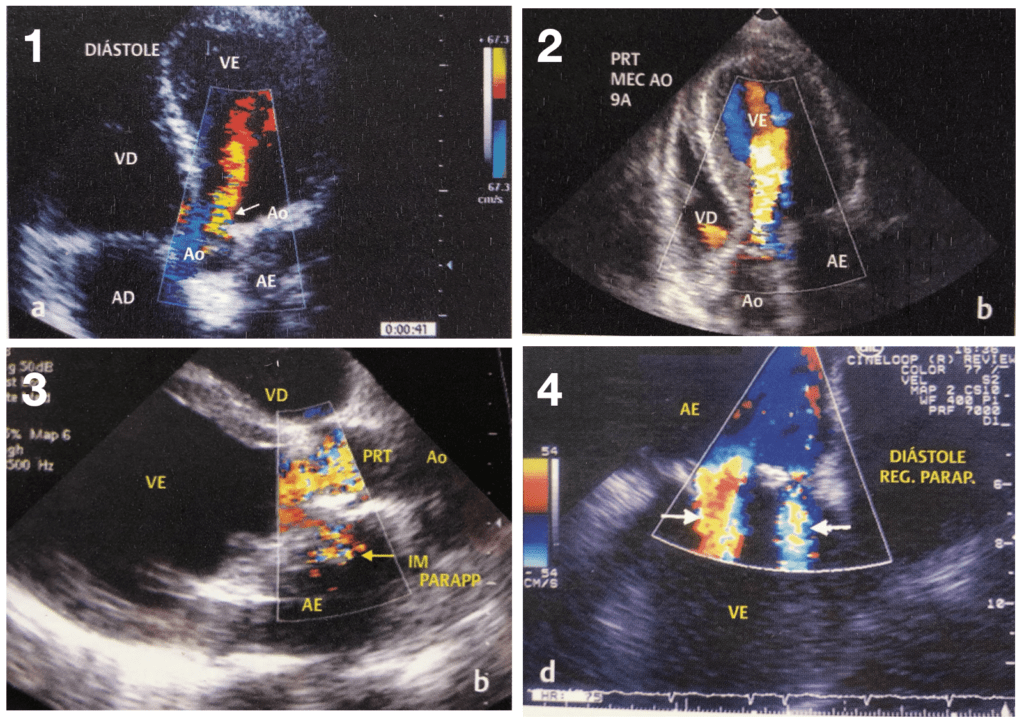
Mismatch
Casos em que próteses normofuncionantes apresentam na fase pós operatória gradientes hemodinâmicos acima do esperado para aquele modelo e tamanho de valva implantada. Isso ocorre por causa de o orifício efetivo da prótese ser pequeno em relação à superfície corporal do paciente;
Disfunção estrutural primária
Os defeitos estruturais são mais comuns nas biopróteses que nas próteses mecânicas, estando, na maioria das vezes, relacionados com o tempo de implante. Podemos citar: calcificação dos folhetos com restrição da sua mobilidade ou mesmo ruptura cuja incidência aumenta com a idade da prótese e geralmente ocorre adjacente à região de uma calcificação.
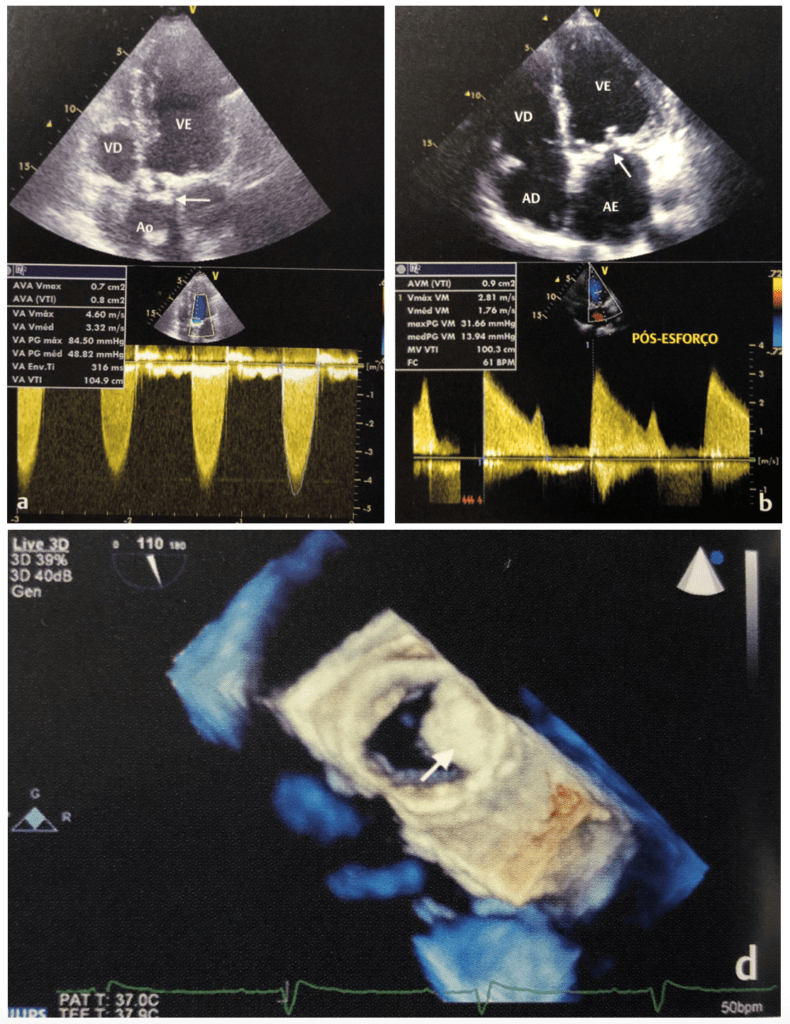
Trombose
As complicações de tromboembolismo são as maiores causas de morbidade em pacientes portadores de próteses cardíacas e a incidência estimada de eventos clínicos varia entre 0,6 a 2,3% por paciente/ano. Essas complicações vão desde trombose protética até eventos embólicos centrais ou periféricos. Os fatores associados ao aumento do risco de tromboembolismo são: FA, dilatação do AE, aumento e/ou disfunção do VE e anticoagulação inadequada.
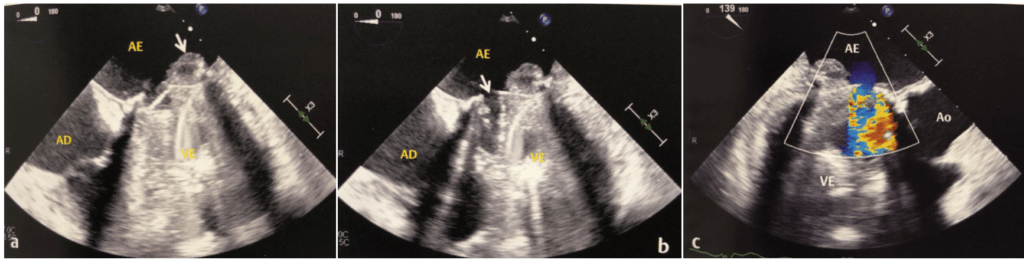
Strands
São imagens filiformes aderidas às próteses descritas como fibrin strands (franjas de fibrina). São estruturas formadas por finos filamentos que pode medir vários milímetros de comprimento e apresentam mobilidade independente da prótese, podendo ser encontradas nos elementos móveis ou região perianular das próteses biológicas ou mecânicas normofuncionantes. Sua incidência é maior em posição mitral e podem ocorrer em pacientes anticoagulados, fato este que sugere que essas estruturas não são compostas apenas de trombos.
Endocardite Infecciosa
Massas de ecos móveis, pedunculadas e presas aos folhetos na presença de um contexto clínico de infecção. As infecções das próteses mitrais frequentemente se estendem além do anel para o tecido perianular e para a fibrosa intervalvar mitroaórtica, podendo causar abscessos anulares, abscessos septais, pericardite, trajetos fistulosos e deiscência da prótese, com regurgitação valvar de importante repercussão hemodinâmica.
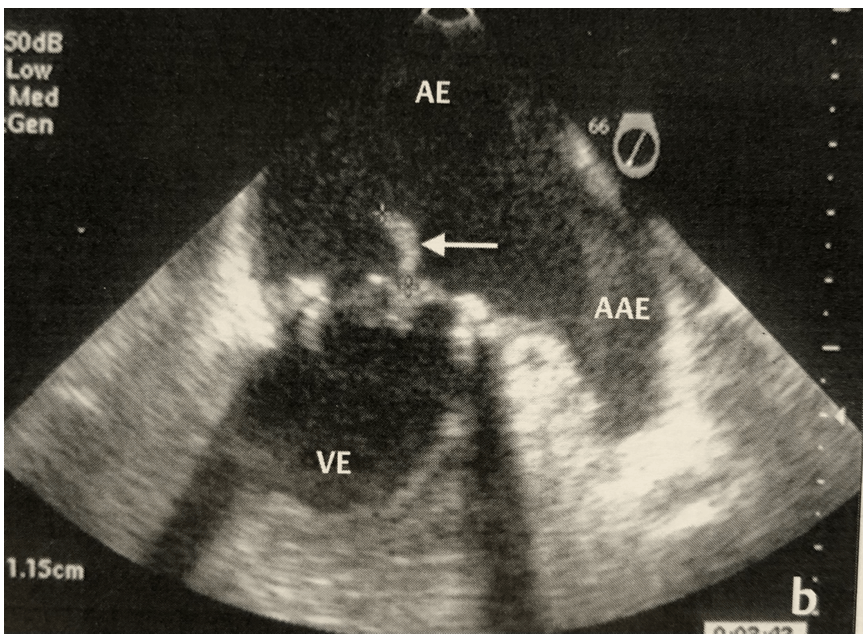
Pseudoaneurisma
O pseudoaneurisma da fibrose mitroaórtica é uma complicação rara após implante protético. Ocorre uma fragilidade e dilatação do tecido fibroso que forma a junção entre o anel mitral anterior e o anel aórtico posterior. Os achados são de uma formação sacular entre a aorta e o AE que se comunica com o VE. A causa mais frequente que leva à formação destes pseuaneurismas é a endocardite infecciosa.

Deiscência
Geralmente, decorrente da soltura de um ou mais pontos na região de fixação do anel. A causa pode ser infecciosa, técnica cirúrgica inadequada ou fragilidade do tecido do paciente. Quando ocorre ruptura de vários pontos, a prótese pode se desprender parcialmente do anel, apresentando um movimento peduncular.
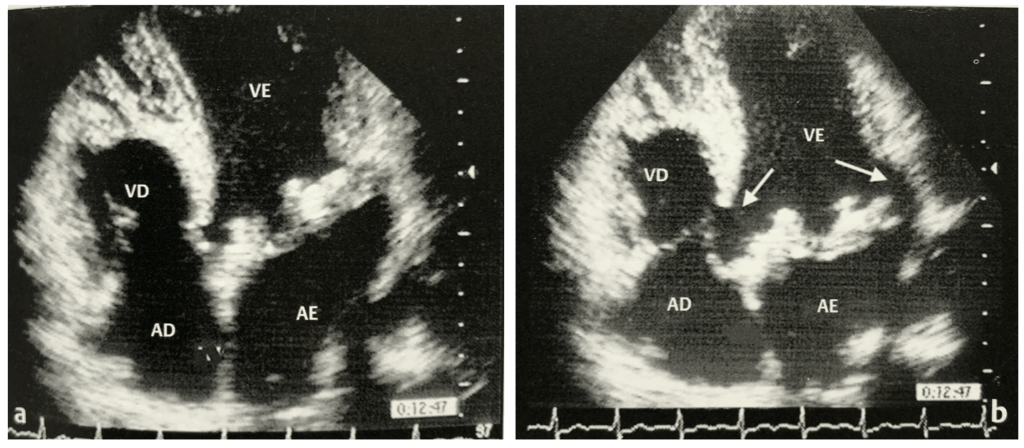
Pannus
Crescimento de tecido fibroso em volta e no interior do anel da prótese, interferindo na mobilidade do seu componente móvel. Por causa do crescimento deste tecido ser lento, esta complicação é tardia, raramente acontecendo antes dos seis meses pós implante da prótese. O principal diagnóstico diferencial é trombose.
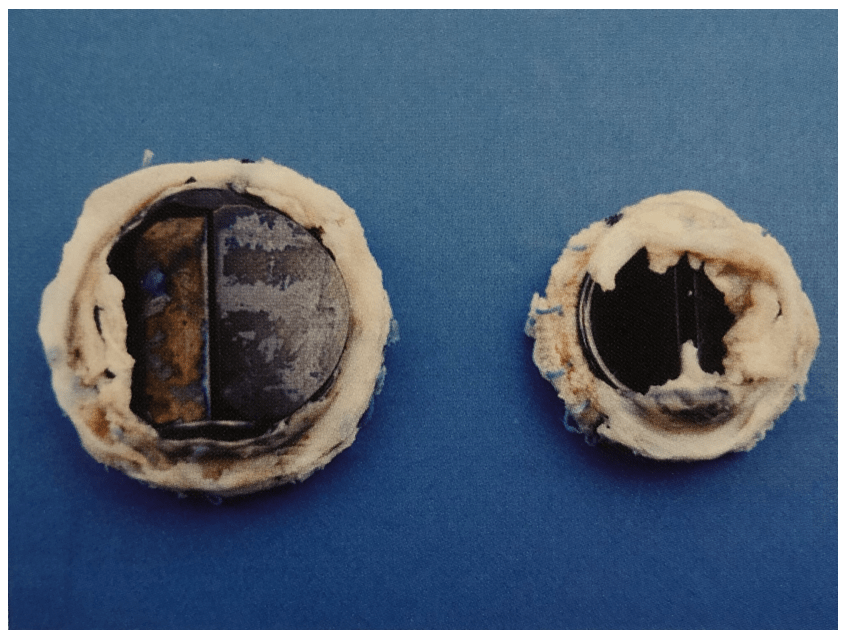
Hemólise
Decorre da destruição mecânica das hemácias por trauma. Graus leves de hemólise podem estar presentes em até 50% dos pacientes portadores de próteses mecânicas normofuncionantes.
Com esta postagem, terminamos a série sobre próteses valvares cardíacas. Se você tem alguma sugestão de temas para abordarmos aqui no blog, sua opinião será muito bem vinda.
Para mais conteúdo como esse, continue acompanhando nosso blog!
Graduado em medicina pela Universidade Potiguar (UnP). Possui residência em Clínica Médica pelo Hospital Universitário Onofre Lopes – HUOL (UFRN) e em Cardiologia pelo Procape – UPE. Porta o título de especialista em Cardiologia pela Sociedade Brasileira de Cardiologia (SBC) e é pós-graduado em Ecocardiografia, pela ECOPE.
Excelente Caio. Parabéns! Djair
Parabéns pelo artigo e também por todo o blog. Vocês são feras…