SOUZA, Alexandre Magno da Rocha Passos.
BARROS, Katarina
Tópicos
Introdução
Diabetes mellitus (DM) é um importante e crescente problema de saúde para todos os países, independentemente do seu grau de desenvolvimento. Em 2017, a Federação Internacional de Diabetes (International Diabetes Federation, IDF) estimou que 8,8% (intervalo de confiança [IC] de 95%: 7,2 a 11,3) da população mundial com 20 a 79 anos de idade (424,9 milhões de pessoas) vivia com diabetes. Se as tendências atuais persistirem, o número de pessoas com diabetes foi projetado para ser superior a 628,6 milhões em 2045. Cerca de 79% dos casos vivem em países em desenvolvimento, nos quais deverá ocorrer o maior aumento dos casos de diabetes nas próximas décadas. O aumento da prevalência do diabetes está associado a diversos fatores, como rápida urbanização, transição epidemiológica, transição nutricional, maior frequência de estilo de vida sedentário, maior frequência de excesso de peso, crescimento e envelhecimento populacional e, também, à maior sobrevida dos indivíduos com diabetes.
Diabetes e suas complicações constituem as principais causas de mortalidade precoce na maioria dos países; aproximadamente 4 milhões de pessoas com idade entre 20 e 79 anos morreram por diabetes em 2015, o equivalente a um óbito a cada 8 segundos. Doença cardiovascular é a principal causa de óbito entre as pessoas com diabetes, sendo responsável por aproximadamente metade dos óbitos por diabetes na maioria dos países¹.
A insuficiência cardíaca (IC) tem uma posição de destaque no grupo das doenças cardiovasculares, ela é definida pelas diretrizes brasileira e europeia como uma síndrome clínica complexa, na qual o coração é incapaz de bombear sangue de forma a atender às necessidades metabólicas tissulares, ou pode fazê-lo somente com elevadas pressões de enchimento. Tal síndrome pode ser causada por alterações estruturais ou funcionais cardíacas e caracteriza-se por sinais e sintomas típicos, que resultam da redução no débito cardíaco e/ou das elevadas pressões de enchimento no repouso ou no esforço². A despeito de avanços na terapêutica da IC, a síndrome mantém-se como patologia grave, afetando, no mundo, mais de 23 milhões de pessoas. A sobrevida após 5 anos de diagnóstico pode ser de apenas 35%, com prevalência que aumenta conforme a faixa etária (aproximadamente de 1% em indivíduos com idade entre 55 e 64 anos, chegando a 17,4% naqueles com idade maior ou igual a 85 anos).³
O DM é um fator de risco independente para o desenvolvimento de IC. O estudo de Framingham documentou um aumento de 2,4 vezes na incidência de IC sintomática nos homens com DM e de 5 vezes nas mulheres com a doença, independentemente da coexistência de hipertensão arterial sistêmica ou doença arterial coronariana, destacando uma discrepância de sexo que não é completamente compreendida. A frequência de IC nos pacientes de DM é maior em relação aos não afetados por DM.4
O aumento da incidência de IC em pacientes diabéticos persiste mesmo após o ajuste para outros fatores de risco, como idade, hipertensão, hipercolesterolemia e doença arterial coronariana. Assim, o termo cardiomiopatia diabética foi cunhado há mais de 40 anos e foi inicialmente usado para descrever disfunção ventricular na ausência de doença arterial coronariana e hipertensão em pacientes diabéticos5 .
Relato de caso
Paciente, 28 anos, sexo masculino, branco. Natural de Santo Antonio de Jesus-BA e procedente da cidade de Wenceslau Guimarães-BA; Agricultor. Portador de diabetes melito do tipo I (DM tipo I) sem etiologia conhecida com diagnóstico aos 12 anos de idade, em insulinoterapia porém com níveis glicêmicos fora da faixa adequada e sem adesão dietética. Encaminhado para serviço de cardiologia geral pelo serviço de endocrinologia por apresentar sinais e sintomas de síndrome de insuficiência cardíaca e exames complementares com achados patológicos.
Queixa de dispneia progressiva iniciada há 6 meses, apresentando naquele momento aos mínimos esforços habituais limitando assim sua atividade ocupacional, assim como ortopneia, bendopneia e dispneia paroxística noturna, além de empachamento pós prandial. Ao exame físico cardiovascular, conformação torácica normal, ictus cordis visível e palpável em sexto espaço intercostal na interseção com a linha axilar anterior, uma polpa e meia digital; sopro holossistólico graduado em II em uma escala de I-VI, em foco mitral sem irradiações, bulhas rítmicas e taquicárdicas com presença da terceira bulha cardíaca. Adiciona-se ao exame físico: ausculta pulmonar com estertores bolhosos em bases pulmonares, turgência de jugulares avaliada ao decúbito dorsal com cabeceira elevada num ângulo de 45°. Pulso radial cheio e simétrico, regular, frequência cardíaca de 101 bpm e níveis pressóricos aferidos em 110×80 mmHg. Saturação periférica de oxigênio de 95% em repouso e ar ambiente. Extremidades com aspecto de boa perfusão, edema de membros inferiores até terço médio, sinal de Godet 3+ numa escala de 1+/4+.
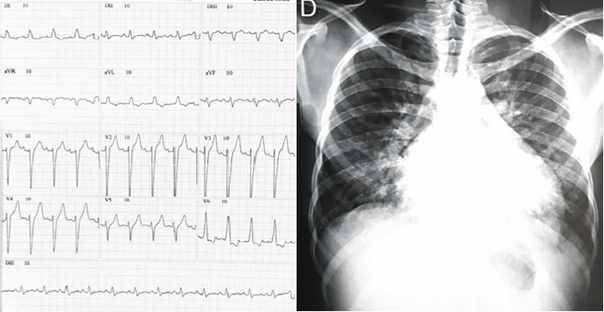
Exames complementares iniciais solicitados conforme anamnese e exame físico; Eletrocardiograma de repouso com 12 derivações (Figura 1) revela ritmo sinusal com batimentos cardíacos regulares, com sinais de sobrecarga de ventrículo esquerdo além de distúrbio de condução pelo feixe His Purkinje caracterizada por bloqueio de completo de ramo esquerdo. Em radiografia do tórax em projeção póstero-anterior (Figura 2), nota-se uma cardiomegalia estimada pelo índice cardiotorácico. Sorologia para doença de Chagas pelo de quimioluminecência e imunofluorência indireta sérica negativa.
Optado por estratificação e rastreio etiológico da síndrome de insuficiência cardíaca com ecodopplercardiograma colorido bidimensional. Ao tal estudo concluiu-se que morfologicamente trata-se de uma cardiopatia dilatada caracterizada por diâmetros e volumes ventriculares esquerdo (VE) e direito além de imagem de “pinheiro tombado” ao modo-M na janela paraesternal eixo longo ao nível do plano valvar mitral, assim como padrão de hipertrofia excêntrica do VE. A disfunção sistólica do VE avaliada pelo método de Simpson está classificada como leve (Fração de ejeção do ventrículo esquerdo de 41,8%) secundária à hipocinesia difusa (figuras 3, 4 e 5). Aumento da pressão de enchimento ventricular traduzido por uma disfunção diastólica do tipo III ou restritiva, E/A de 3,7; E/e’ média de 14,9; estimando uma pressão de venocapilar pulmonar de 20,4 mmHg (figuras 6, 7 e 8). Inclui-se regurgitação tricúspide com velocidade máxima de 3,3 m/s garantindo um gradiente entre as câmaras direitas de 44,5 mmHg. Pressão sistólica na artéria pulmonar calculada em 59,5 mmHg sabendo que a pressão estimada de átrio direito, através da variação ventilatória dos diâmetros da veia cava inferior, 15 mmHg. Átrio esquerdo encontrava-se com aumento importante de seu volume indexado (figura 9), as regurgitações das valvas atrioventriculares foram classificadas como secundárias e grau moderado. Função sistólica do ventrículo direito preservada avaliada pela TAPSE (excursão sistólica do anel da valva tricúspide) e pela velocidade da onda S’ do anel tricúspide (Figuras 10e 11). Septos íntegros, ausência de derrame pericárdico e trombos ou tumores intracavitários.
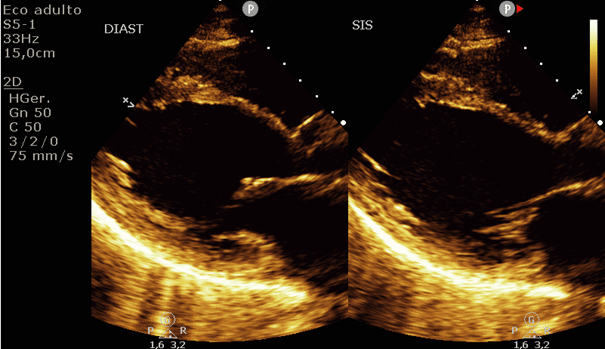
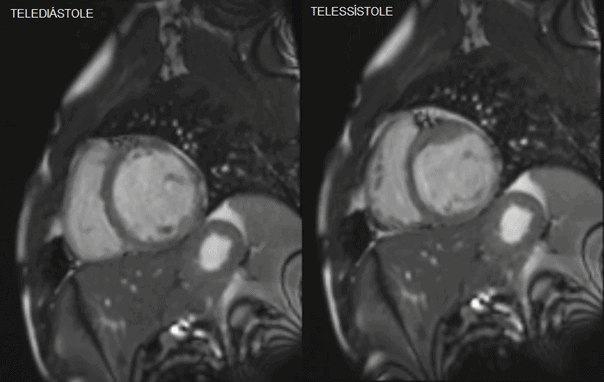
Figura 3: Corte paraesternal eixo longo, ventrículo esquerdo em telediástole (esquerda) e telessístole (direita)
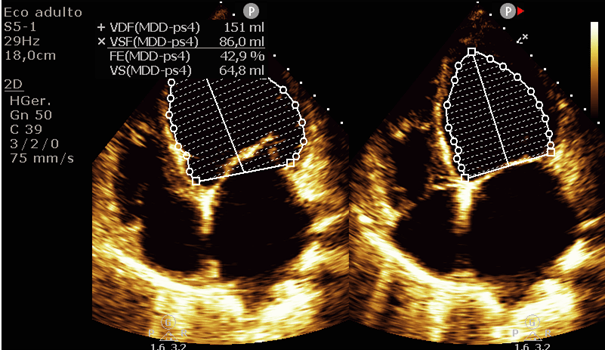
Figura 4: Volumes telediastólico (esquerda) e telessistólico (direita) no corte apical quatro câmaras – Método de Simpson.
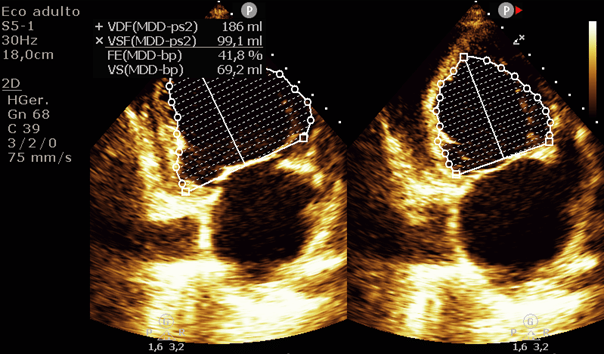
Figura 5: Volumes telediastólico (esquerda) e telessistólico (direita) no corte apical duas câmaras – Método de Simpson.
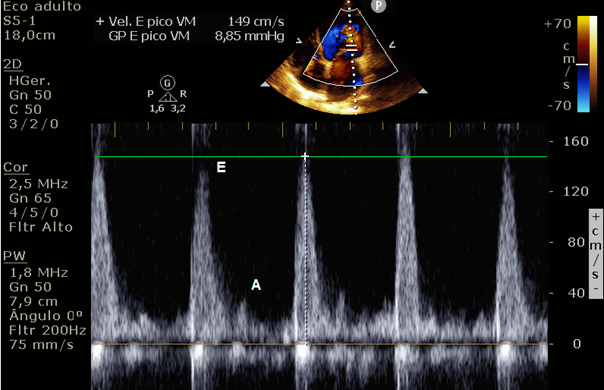
Figura 6: Doppler transvalvar mitral, ondas E e A.
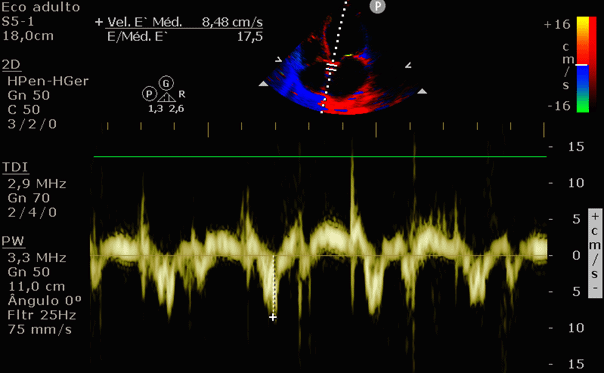
Figura 7: Doppler tecidual, onda e’ do anel mitral lateral.
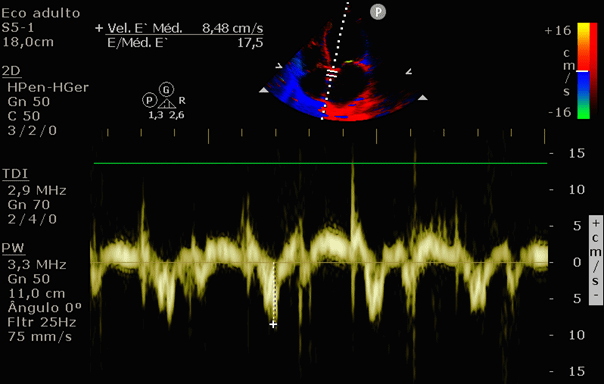
Figura 8: Doppler tecidual, onda e’ do anel mitral medial (septal).
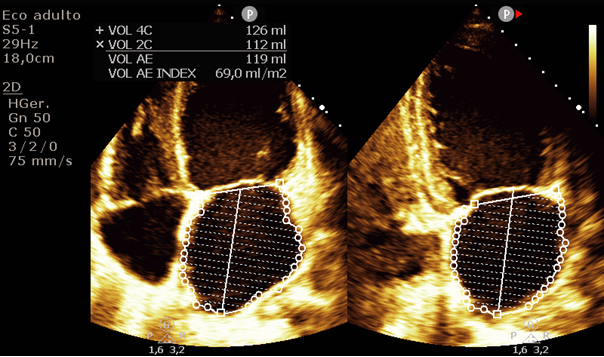
Figura 9: Volume de átrio esquerdo biplanar.
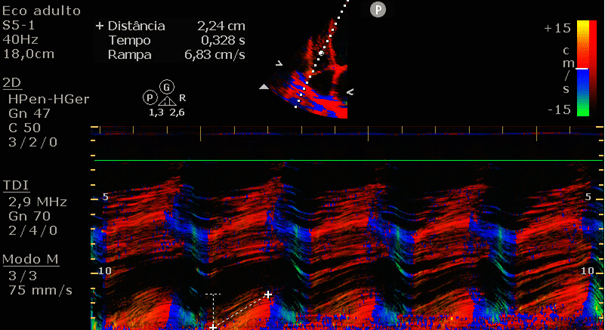
Figura 10: TAPSE

Figura 11: Onda S’ do anel tricúspide lateral.
Diante de uma cardiopatia dilatada de fração de ejeção reduzida sintomática em individuo jovem, sem sinais e sintomas de doença arterial coronariana, níveis pressóricos normais, sem evidência sorológica de doença de Chagas; prosseguiu-se screening da etiologia de tal síndrome. Realizada ressonância nuclear magnética de coração após 7 meses da primeira consulta em serviço de cardiologia, ao laudo dessa temos: Miocardiopatia de provável etiologia isquêmica com função sistólica do ventrículo esquerdo reduzida de grau moderado – Fração de ejeção de 33,1% – (Figura 12) à custa do defeito segmentar (hipocinesia do segmento apical das paredes lateral e inferior, acinesia do segmento médio da parede anterolateral, hipocinesia do segmento médio das paredes inferolateral e inferior, acinesia do segmento basal das paredes anterolateral e inferolateral, e hipocinesia do segmento basal da parede inferior; normocinesia dos demais segmentos), dilatação importante das câmaras esquerdas, infarto do miocárdio em território lateral.
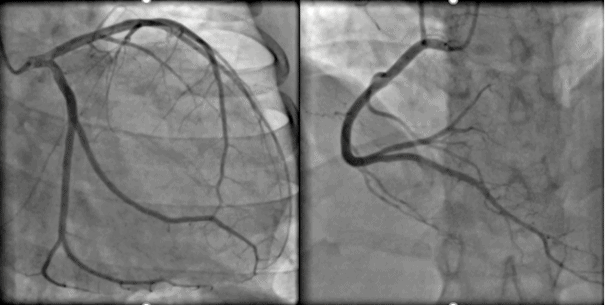
O estudo da anatomia coronariana neste caso foi de forma invasiva com cineangiocoronariografia. Essa sem evidências angiográficas de aterosclerose com comprometimento obstrutivo assim como trombos, origens e trajetos habituais das artérias coronarianas epicárdicas (Figura 13).
Discussão
O cardiomiopatia diabética (CD) surge como uma entidade etiológica de insuficiência cardíaca no ano de 1972 através de estudos post mortem de 04 pacientes, sendo confirmada no estudo de Framingham heart study no ano de 1974. Pelas sociedades de cardiologia norte-americanas e europeia, definiu-se em 2013 como uma condição clínica de disfunção ventricular que ocorre na ausência de aterosclerose coronariana e hipertensão arterial sistêmica em pacientes portadores de DM.
É caracterizada fisiopatologicamente pela disfunção diastólica do ventrículo esquerdo além da fibrose miocárdica. A lesão miocárdica nos estudos anatomopatológicos é composta por hipertrofia miocárdica, depleção de miofibrilas, fibrose intersticial, espessamento da membrana basal de pequenos vasos, aumento da matriz e da membrana basal das arteríolas e microangiopatia intramiocárdica.
Tal lesão não tem uma única causa e é resultado de anormalidades metabólicas relacionadas com o DM (Figura 14), são elas: hiperglicemia, ácidos graxos livres e a resistência insulínica. Esses, são desencadeadores do aumento do estresse oxidativo e ativação da proteína quinase C assim como dos produtos da glicosilação avançada além da estimulação dos sistemas renina-angiotensina-aldosterona e nervoso simpático.
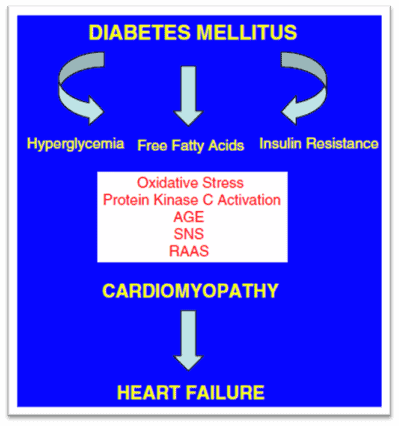
Figura 14: Fisiopatologia da cardiomiopatia diabética e da insuficiência cardíaca.
Giles TD et al., 2004.
A disfunção diastólica do ventrículo esquerdo que está relacionada com depósito de colágeno e fibrose miocárdica do VE que está relacionada com depósito de colágeno e fibrose do VE e ocorrem ainda no estágio de pré DM (15 semanas antes do diagnóstico) na fase de resistência insulínica.
Em abril de 2020, Cieluch e colaboradores da Universidade de Ciências Médicas de Poznan (Polônia) descreve em artigo de revisão uma evidência descrita como robusta entre disfunção mitocondrial na patogênese da CD especificamente em pacientes diabéticos do tipo I. ainda em 2020, em artigo de revisão de Tadic M. adiciona a disfunção mitocondrial além de disfunção endotelial e redução da síntese do óxido nítrico coronariano como mecanismos de lesão miocárdica; e estratifica em seis diferentes estágios da CD.
Estágio I é composto por inflamação e fibrose intersticial; hipertrofia, apoptose e necrose de cardiomiócito. Diminuição da complacência cardíaca e arterial, aumento da pós carga. Estágio II e III: dano mecânico do VE e disfunção diastólica. Estágio IV: hipertrofia do VE. Estágio V: insuficiência cardíaca de fração de ejeção preservada. Estágio VI: insuficiência cardíaca de fração de ejeção reduzida.
Tal estratificação torna-se útil pois, o primeiro estágio só é detectável com ressonância magnética miocárdica na sequência T1 que é o padrão ouro na avaliação de fibrose miocárdica pois distingue o tecido normal do fibrótico. Considera-se o fato que neste estágio a CD é reversível, isso é de grande importância para iniciar o adequado tratamento assim que possível. Com a dificuldade de acesso ao tal método, Flores-Ramirez e colaboradores da universidade autônoma de Nuevo Leon no México propôs o uso da Galactin-3 (Gal-3) como biomarcador precoce da CD.
Tadic M. conclui que o ecocardiograma convencional é útil na avaliação de CD nas fases a partir da III (disfunção diastólica) e além da aplicabilidade da técnica despeckle tracking no estágio II.
TD Giles et al citam que a adição do doppler tecidual ao Doppler transvalvar da valva mitral convencional (relação das velocidades de pico das ondas E e A, tempo de desaceleração, tempo de relaxamento isovolumétrico) foi capaz de demonstrar disfunção diastólica em 75% de 57 pacientes assintomáticos, normotensos e diabéticos.
Helena Kenny e Dale Abel, em janeiro de 2019, revisaram a IC em pacientes diabéticos com foco no tratamento medicamentoso. Das sete classes farmacológicas para tratamento da DM2, acende-se o destaque para a classe dos inibidores do SGLT-2. Representados pela Canaglifozina, Dapaglifozina e Empaglifozina, estes atuam promovendo glicosúria sendo efetivos no controle glicêmico tanto em monoterapia quanto combinado. Naquele momento, dados do CANVAS trial e EMPAREG outcome trial foram suficientes para classificar tal grupo farmacológico como a primeira classe de antidiabéticos orais que definitivamente reduz o risco de IC na DM2 por aumento da natriurese, redução de níveis pressóricos, proteção renal.
Já em 2020, dois estudos foram divulgados: EMPEROR-Reduced (Empaglifozina) e DAPA-HF (Dapaglifozina). Ambas foram testadas em pacientes portadores de IC de fração de ejeção reduzida. Em metanálise utlizando os dados de 8474 pacientes dos dois estudos citados, Zannad et al concluiram que tais medicações reduzem mortalidade por todas as causas (redução de 13%, HR 0·87, 95% CI 0·77–0·98; p=0·018) assim como a mortalidade cardiovascular (redução de 14% HR 0·86, CI 0·76–0·98; p=0·027).
Retomando ao paciente do relato de caso, trata-se assim de indivíduo normotenso portador de diabetes melitus tipo I sem controle adequado que evolui com síndrome de insuficiência cardíaca, ecocardiograma evidenciou disfunções sistólica e diastólica do ventrículo esquerdo, sorologias para T.Cruzi negativas. Ressonância nuclear magnética detecta disfunção sistólica global e segmentar com área de infarto miocárdico, porém cineangiocoronariografia não descreve lesões obstrutivas. Por exclusão, o diagnóstico etiológico de tal síndrome é a cardiopatia diabética estágio VI.
Conclusão
DM está longe de ser uma doença apenas metabólica mas também uma condição cardiovascular, por isso, cardiologistas devem estar atualizados e comprometidos na prevenção, diagnóstico, tratamento e no rastreio de lesões de órgãos alvos. Ao diagnóstico sindrômico de IC, é fundamental a busca do diagnóstico etiológico. Tratamentos direcionados por etiologia reduzem mortalidade e melhoram a qualidade de vida.
Referências bibliográficas
1-DIRETRIZES. Sociedade brasileira de diabetes: 2019-2020.
2-GUIDELINES FOR DIAGNOSIS AND TREATMENT OF ACUTE AND CHRONIC HEART FAILURE, European heart journal, 2016.
3-DIRETRIZ BRASILEIRA DE INSUFICIÊNCIA CRÔNICA E AGUDA, arquivos brasileiros de cardiologia, 2018.
4-KENNY, H.C; DALE ABEL, E. Heart failure in type 2 diabetes mellitus: impact of glucose-lowering agentes, heart failure therapies, and novel therapeutic strategies.Circulation researsh, 2019.
5-BARRETTO, A.C.P; DEL CARLO, C.H: Cardiomiopatia diabética e insuficiência cardíaca no portador de diabetes; Diabetes mellitus, uma abordagem cardiovascular. Clannad, 2019.
6-OKOCHI, K. Miocardiopatia diabética, artigo de revisão. Arquivos endocrinologia e metabologia, 2007.
7-GILES, T.D. Diabetes mellitus and heart failure: basic mechanism, clinical features,and therapeutic considerations, Cardiology clinics, 2004.
8-ZANNAD, F. SGLT2 inhibitors in patients with heart failure with reduction ejection fraction: a meta-analysis of the EMPEROR-reduced and DAPA-HF trials. The Lancet, 2020.
9-TADIC, M. Diabetic cardiomyopathy: How can cardiac magnetic ressonance help? Acta diabetologica, 2020.
10-CIELUCH, A. Can we prevent mitochondrial dysfunction and diabetic cardiomyopathy in type 1 diabetes mellitus? Pathophysiology and treatment options. International journal of molecular Science. 2020.
11-FLORES-RAMIREZ, R. Global longitudinal strain as a biomarker of diabetic cardiomyopathy. A comparative study with Gal-3 in patients with preserved ejection fraction. Archivos de cardiologia de Mexico, 2016.
Para mais conteúdo como esse, continue acompanhando nosso blog!
Excelente. Ótima atualização.