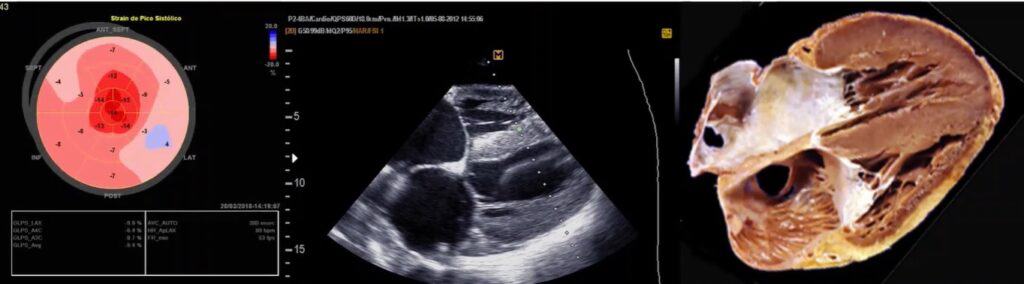
As miocardiopatias restritivas e infiltrativas podem ter origem genética ou adquirida. Geralmente, resultam em fibrose miocárdica, regional ou difusa, tendo como padrão ouro para seu diagnóstico a biópsia endomiocárdica. O método complementar que mais se aproxima da biópsia é a ressonância nuclear magnética, que oferece alta sensibilidade, não utiliza radiação ionizante, quantifica fluxos e fibrose miocárdica, assim como emprega contraste de baixa toxicidade. Entre algumas inconveniências do método estão: baixa disponibilidade e alto custo do exame, impossibilidade de realização em pacientes instáveis e contraindicação na presença de alguns dispositivos (como grampos intracerebrais, marcapassos mais antigos ou dispositivos cocleares).
A ecocardiografia, por sua vez, oferece algumas vantagens na avaliação destes pacientes. Através dela, podemos obter dados como: função diastólica, avaliação da repercussão hemodinâmica (aumento dos átrios, função ventricular), avaliação do comprometimento valvar e diagnóstico diferencial com pericardite constritiva (em que o doppler tecidual é normal, a velocidade de propagação do fluxo mitral é normal ou aumentada e existe variação respiratória dos fluxos transvalvares).
A seguir, vamos discutir como podemos utilizar o strain como mais uma aliada diagnóstica, evolutiva e prognóstica de algumas das principais cardiopatias restritivas e infiltrativas encontradas na prática clínica.
Tópicos
Amiloidose
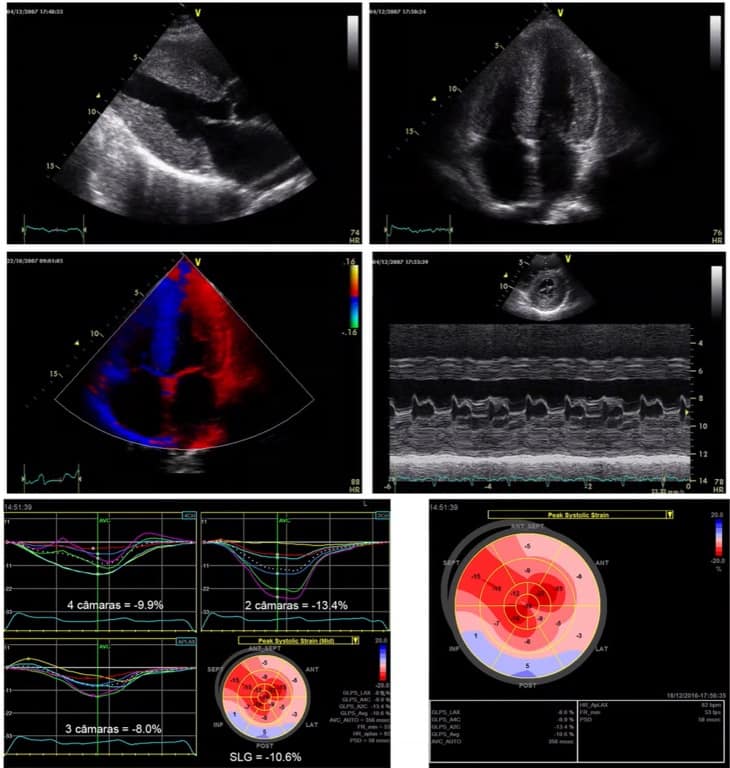
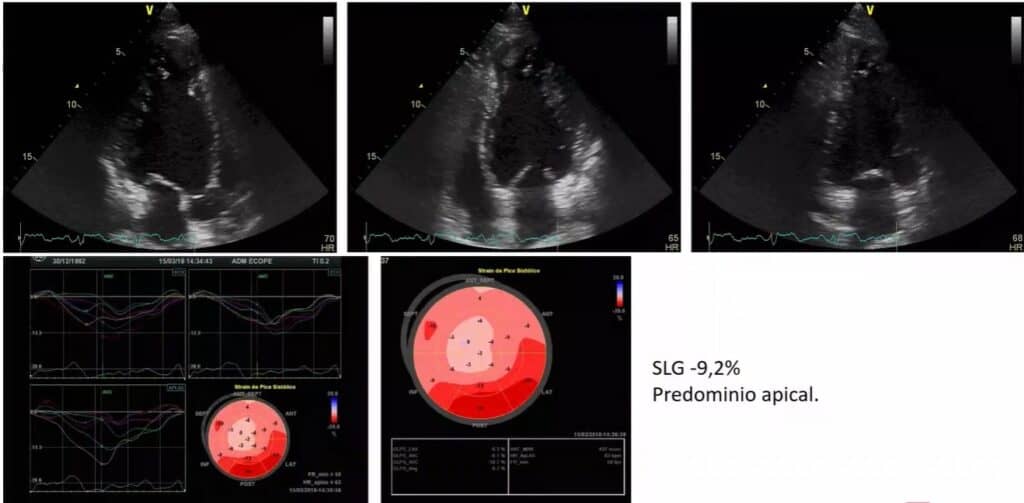
Na figura 3, temos um paciente com diagnóstico de amiloidose. Percebemos o aumento da espessura e ecogenicidade das paredes ventriculares e atriais, redução do Doppler tecidual difusamente (devido a infiltração e fibrose do miocárdio, comprometendo o trabalho cardíaco), o aspecto de hipocontratilidade difusa e de múltiplas camadas das paredes do ventrículo esquerdo (VE) ao modo-M, redução do Strain Longitudinal Global (SLG) do VE, com relativa preservação apical (apical sparing) no mapa polar, achado característico desta doença (porém não exclusivo, estando presente em outras cardiopatias, conforme vimos nos posts anteriores).
Sarcoidose
Doença infiltrativas por granulomas não caseosos, evoluindo com 2 padrões de apresentação mais comuns: 1) Tipo 1: acomete as regiões basais das paredes ântero-septal e ínfero-septal; 2) Tipo 2: acomete as regiões basal e medial da parede ínfero-lateral e médio-apical da parede inferior.
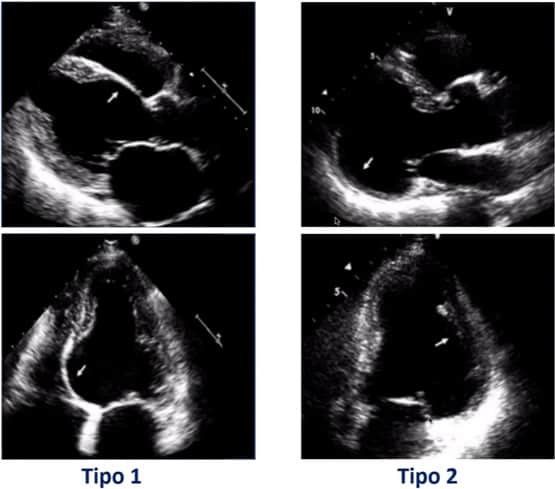
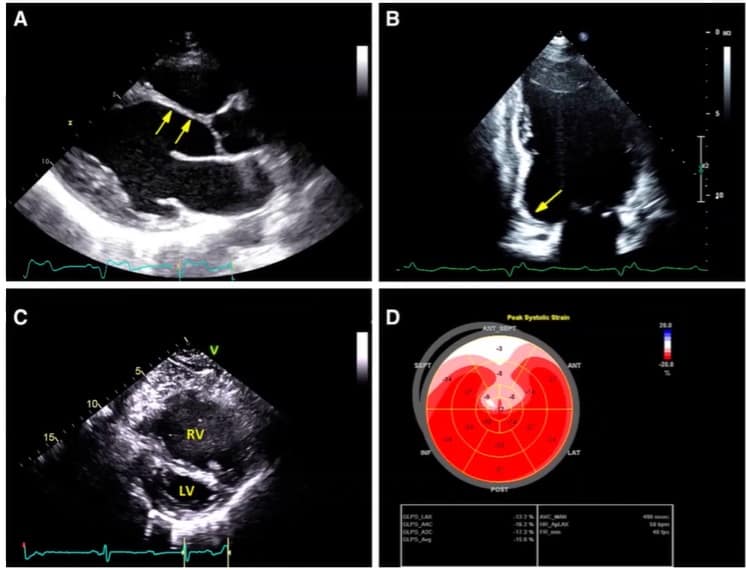
Na figura 5, temos o exemplo de um paciente com o tipo 1 da doença, com fibrose da parede ântero-septal basal, com mapa polar do SLG mostrando redução do trabalho cardíaco na referida região.
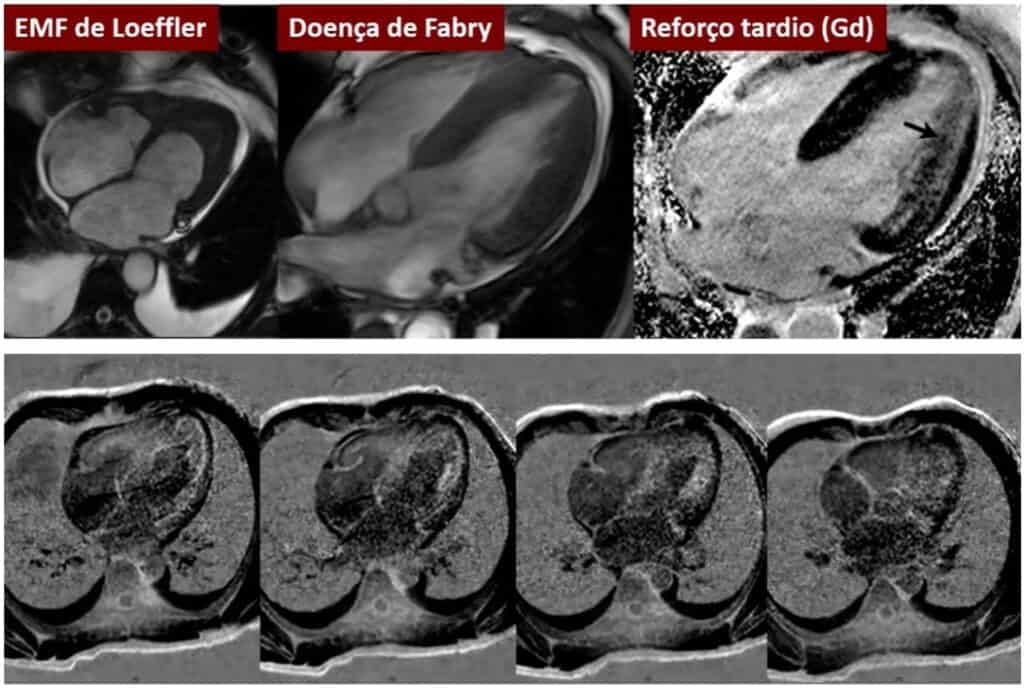
Doença de Fabry
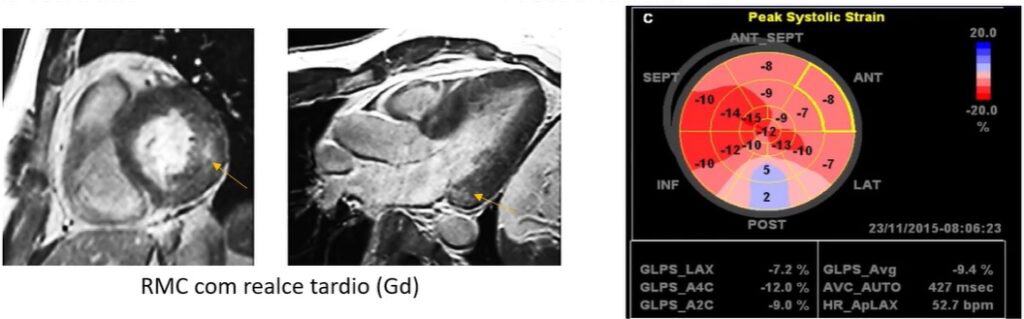
Doença de depósito dos lisossomos, os pacientes evoluem com hipertrofia miocárdica, fibrose, insuficiência cardíaca e arritmias. Observamos acometimento regional da deformação miocárdica, sendo a região ínfero-lateral a localização mais frequente, como mostrada na figura 6.
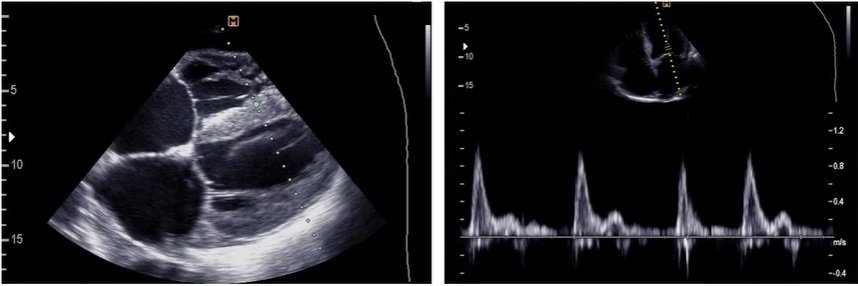
Endomiocardiofibrose
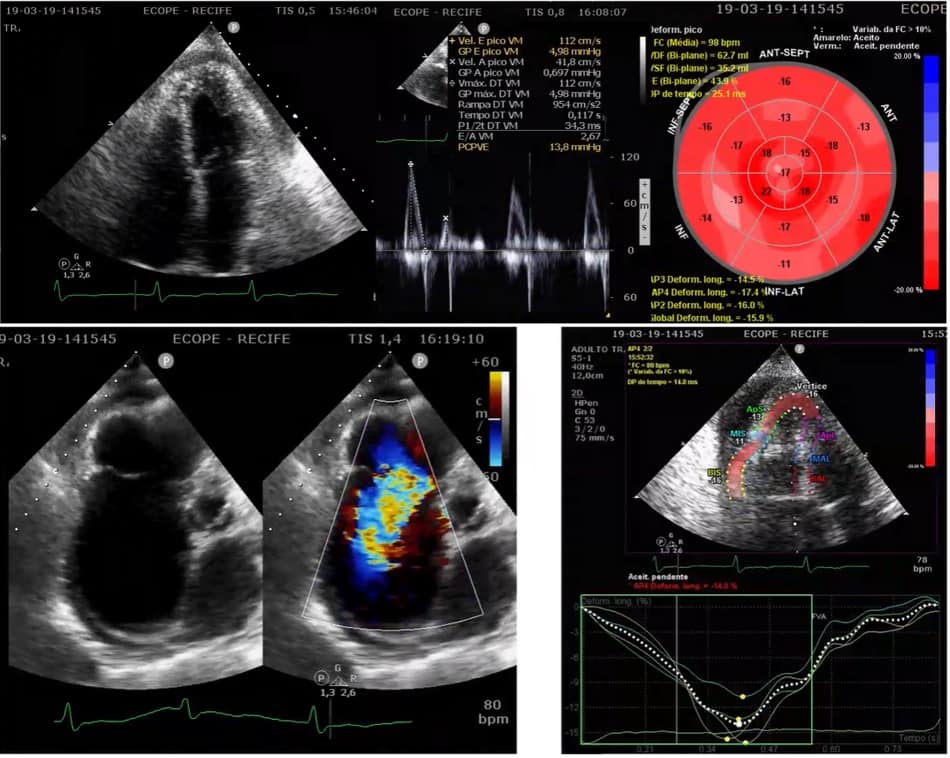
Existe fibrose endocárdica, com frequente envolvimento valvar. Desta forma, normalmente constatamos à ecocardiografia a obliteração fibro-trombótica dos ápices ventriculares (podendo acometer um ventrículo ou os dois), refluxos valvares e grandes dilatações atriais. Como o músculo abaixo da fibrose é relativamente preservado, o SLG pode estar reduzido difusamente (sem evidência de comprometimento regional) até normal, e não há evidências de dissincronias significativas entre os segmentos ventriculares.
Miocárdio Não Compactado
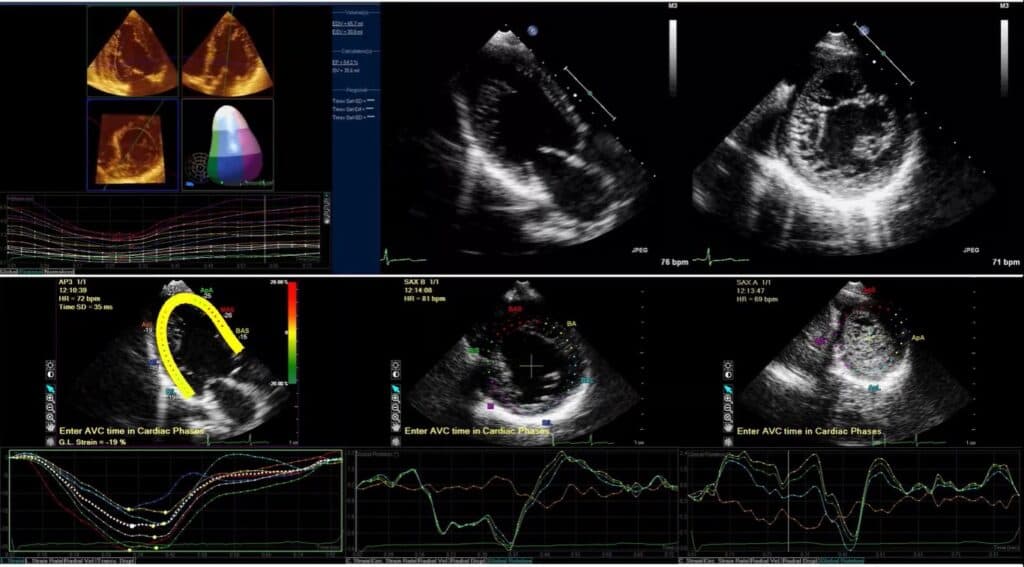
O critério diagnóstico utilizado na ecocardiografia é uma relação entre as espessuras das paredes não compactada e compactada maior que 2,4 (na ressonância nuclear magnética, esta relação cai para 2,3). Existe um desarranjo ventricular com o aumento da trabeculação das paredes, o que pode levar a dilatação das câmaras, perda de função contrátil, fibrose, arritmias e fenômenos tromboembólicos (devido a estase sanguínea intratrabecular, o que favorece a formação de trombos). O padrão do mapa polar nessa cardiopatia é controverso, podendo ou não haver preservação apical relativa.
Uma utilização interessante do Strain nestes pacientes é a análise da rotação basal, apical e do twist. A redução da rotação das paredes e a rotação apical reversa (achado específico preditor de complicações da doença) podem estar presentes inclusive em pacientes assintomáticos, com câmaras de dimensões normais e função sistodiastólica normal.
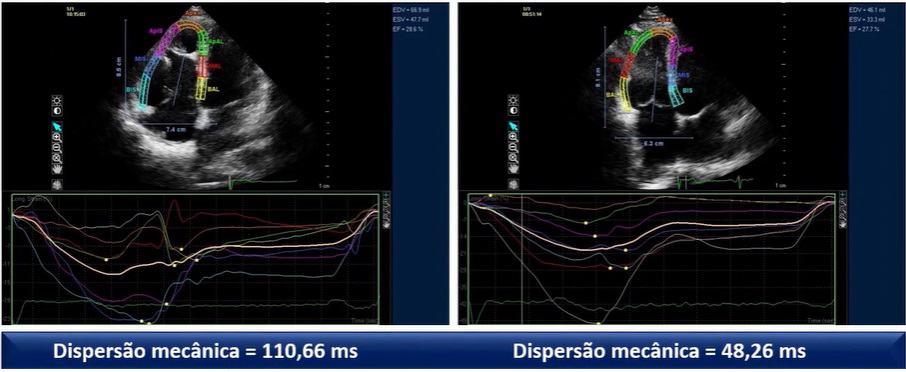
Displasia Arritmogênica do Ventrículo Direito
O estudo da dispersão mecânica da parede livre do ventrículo direito pode funcionar como preditor de eventos arrítmicos em pacientes com doença sintomática ou assintomática, sugerindo que esta ferramenta pode ser utilizada para estratificação de risco dos pacientes e prescrição de terapias profiláticas.
Gostaram do post? Comentem, discutam, compartilhem e tirem suas dúvidas. Na próxima semana, discutiremos um pouco sobre a aplicação do strain nas coronariopatias. Até lá!
Para mais conteúdo como esse, continue acompanhando nosso blog!

Graduada em medicina, pela Universidade Federal de Pernambuco (UFPE). É pós-graduada em Cardiologia, pela Funcordis, e em Ecocardiografia, pela ECOPE. Possui título de Especialista em Cardiologia, pela Sociedade Brasileira de Cardiologia.
Excelente, muito didático. Grato.
Muito obrigada, Alfredo!!! Um abraço!!!
Olá Ana, tenho bicúspidia aórtica, e tenho 36 anos. Há alguns suplementos que me possam ajudar a retardar?
Grato de coração
Olá, Edgar! Infelizmente não existem suplementos ou medidas farmacológicas para retardar o desenvolvimento de complicações. O melhor que você pode fazer é procurar ter hábitos de vida saudáveis, pois doenças como hipertensão, diabetes, dislipidemia, obesidade e o sedentarismo podem contribuir de forma negativa, acelerando o processo de degeneração e desenvolvimento de complicações.
Olá Ana, fico agradecido desde já pela sua atenção e resposta ao meu pedido.
Realmente achava que para além dos hábitos de vida saudaveis, que pudesse haver no seu entendimento algum suplemento natural, coenzimas , resveratrol ou algum tipo de suplemento com provas cientificas crediveis ou mesmo da sua intuição. Quem sabe um dia se lembre ou descubra e se lembre de mim! =) Grato desde já Ana. Saúde da boa para si e tudo de bom.
Disponha, Edgar!!! Também espero que se descubra formas de combate direto ao surgimento de complicações relacionadas a valva aórtica bicúspide. Muita saúde para você e sua família!!! 🙂
Gostei muiiiito , parabéns
Muito obrigada!!!