O Plaque-RADS é um sistema padronizado multimodal (US, CTA e RM) que complementa o grau de estenose ao incorporar características morfológicas e composicionais da placa, com objetivo de estratificar risco de evento cerebrovascular ipsilateral.
Trata-se de uma mudança de paradigma:
Não avaliar apenas o “quanto estreita”, mas “qual é a biologia da placa”.
Estrutura do Plaque-RADS
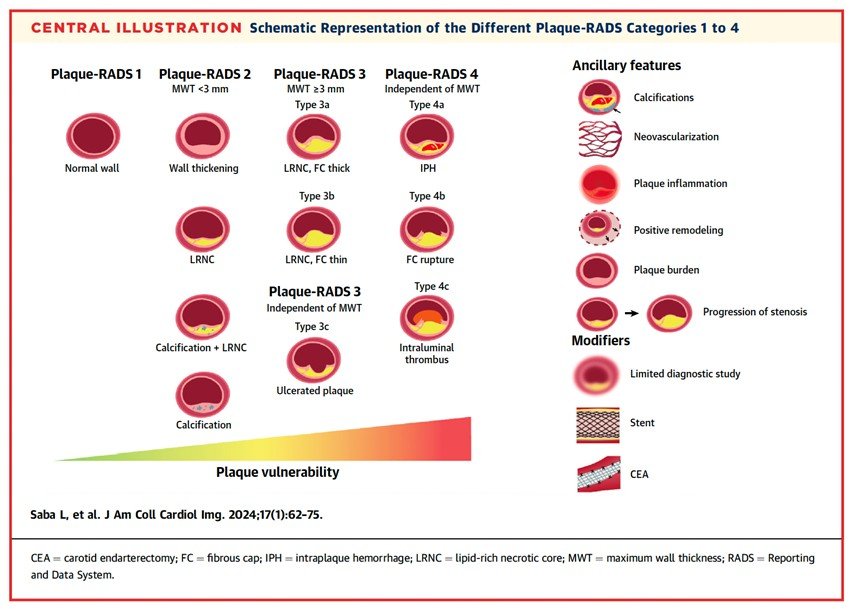
A classificação vai de 1 a 4, com subcategorias (a, b, c) nos graus 3 e 4.
Plaque-RADS 1 – Artéria normal
- Parede regular
- Sem espessamento focal
- CMI < 1,5 mm
- Ausência de placa
Risco atribuível: ausente
Plaque-RADS 2 – Placa inicial (baixo risco)
Critérios:
- Placa excêntrica
- Espessura da placa < 3 mm
- Ausência de:
- Hemorragia intraplaca (HIP)
- Ruptura de capa fibrosa
- Trombo intraluminal
Composição possível:
- Fibrose predominante
- Pequenos focos lipídicos
- Pequenas calcificações
Interpretação clínica: placa estruturalmente estável.
Plaque-RADS 3 – Placa estruturada, sem complicação
Critério principal:
- Espessura da placa ≥ 3 mm
- Ausência de critérios de placa complicada
Subdividido em:
3a – Capa espessa
Características:
- Núcleo lipídico moderado/grande
- Capa fibrosa espessa e íntegra
- Pode haver calcificação
Dados relevantes:
Meta-análise (Gupta et al.) mostrou HR ≈ 3 para eventos quando LRNC presente.
Risco: moderado
3b – Capa fina (ainda íntegra)
- Núcleo lipídico moderado/grande
- Capa fina
- Sem ruptura
Observação importante:
A capacidade de imagem para definir capa fina é limitada.
Na RM, ausência de visualização de capa espessa pode sugerir capa fina.
Risco: maior que 3a, mas ainda sem complicação
3c – Placa ulcerada (sem complicação ativa)
- Ulceração superficial
- Sem HIP
- Sem ruptura evidente
- Sem trombo intraluminal
Representa provável ruptura prévia cicatrizada.
Plaque-RADS 4 – Placa complicada (alto risco)
Independe da espessura da placa. Basta um dos seguintes achados:
4a – Hemorragia intraplaca (IPH)
Marcador mais robusto de vulnerabilidade
Dados:
- Presente em 89% das placas complicadas no CAPIAS
- HR 2,12 para recorrência no estudo PARISK
- HR 11 para recorrência ipsilateral (dados combinados)
- Até 8x maior risco de primeiro AVC em assintomáticos
Identificação por modalidade:
- RM (padrão-ouro)
- T1 hiperintenso
- TOF hiperintenso
- US pode sugerir por áreas hipoecoicas
- CTA pouco sensível
4b – Ruptura da capa fibrosa
- Descontinuidade da capa
- Comunicação entre lúmen e núcleo
- Pode haver hemorragia justaluminal
Meta-análise: HR ≈ 5,9 para eventos com capa fina/rompida.
4c – Trombo intraluminal
Marcador de risco extremamente alto
- Defeito de enchimento (CTA)
- Massa intraluminal em RM
- Áreas ecogênicas móveis no US
OR 103 para AVC de origem carotídea.
Marcadores Auxiliares de Vulnerabilidade
Não definem categoria, mas devem ser relatados, pois esses achados refinam a estratificação:
- Inflamação
- Neovascularização
- Remodelamento positivo
- Progressão da estenose
- Carga de placa
- Calcificação
Como Relatar (Modelo Estruturado)
Sintaxe recomendada:
Lado: % estenose / Modalidade Plaque-RADS / CMI ou espessura da placa / Achados auxiliares / Modificadores
Exemplo:
Carótida direita: 50% / RM Plaque-RADS 4a / Espessura da placa 5 mm / Remodelamento positivo
A medida da espessura deve ser realizada pela visão axial perpendicular ao eixo do vaso e incluir os componentes calcificados e não calcificados.
Reprodutibilidade
Concordância interobservador (kappa):
- US: 0,804
- CTA: 0,868
- RM: 0,876
- Global: 0,856
Excelente aplicabilidade clínica.
Mensagem Clínica Central
O artigo propõe que:
- Estenose isolada não é suficiente.
- A biologia da placa prediz evento.
- HIP e trombo intraluminal são marcadores mais fortes que grau de estenose isolado.
- O sistema padroniza comunicação entre:
- Radiologia
- Cirurgia vascular
- Neurologia
- Pesquisa
Pontos Práticos para Ecografia Vascular
Para o ultrassonografista:
- Medir CMI sistematicamente.
- Avaliar:
- Áreas justaluminais negras
- Ecogenicidade
- Microflow (neovascularização)
- Ulceração > 1 mm
- Suspeitou HIP ou complicação?
Indicar RM.
Conclusão Técnica
O Plaque-RADS propõe um modelo estruturado, multimodal e clinicamente aplicável para:
- Identificação objetiva de placas vulneráveis.
- Estratificação de risco individual.
- Apoio à decisão terapêutica.
Trata-se de um passo importante na integração entre morfologia, imagem e desfecho clínico.
IMPLICAÇÕES CLÍNICAS DO PLAQUE-RADS
Conceito-chave: Estenose ≠ Risco Isolado
Historicamente, a decisão de intervir ou não numa estenose de carótidas baseava-se apenas no grau de estenose provocada por ela. Sendo assim:
- Sintomáticos ≥ 50% → revascularização
- Assintomáticos ≥ 60–70% → decisão individualizada
Com Plaque-RADS, uma placa 40% com HIP (RADS 4a) pode ter risco superior a uma placa 75% fibrosa (RADS 2–3a). Isso muda a hierarquia de risco.
Implicações Terapêuticas por Categoria
Plaque-RADS 1
Conduta:
- Controle de fatores de risco
- Estatina conforme risco global
- Seguimento habitual
Sem indicação de imagem avançada.
Plaque-RADS 2
Placa estruturalmente estável.
Sintomático leve?
- Avaliar causalidade
- Raramente justifica intervenção isoladamente
Assintomático
- Tratamento clínico intensivo
- Estatina de alta potência
- Antiagregação se indicado por risco global
Aqui o papel é preventivo.
Plaque-RADS 3 (placa estruturada, sem complicação ativa)
3a – capa espessa
Implica risco intermediário.
Assintomático 60–69%:
- Tratamento clínico otimizado pode ser suficiente
- Seguimento por imagem mais curto (6–12 meses)
Sintomático < 50%:
- Pode justificar investigação adicional (RM)
- Avaliar outros mecanismos embólicos
3b – capa fina
Biologicamente instável, porém sem ruptura.
Aqui começa a zona cinzenta.
Em paciente sintomático:
- Mesmo com estenose moderada, pode haver benefício em CEA
- Especialmente se idade < 75 anos
Em assintomático:
- Não há consenso formal
- Pode justificar intensificação terapêutica agressiva
- Considerar discussão multidisciplinar
3c – Ulceração cicatrizada
Se estenose ≥ 50% e sintomático: Tendência a indicar revascularização
Se assintomático: Avaliar outros marcadores (progressão, microembolização)
Plaque-RADS 4 – Alto Risco
Aqui a discussão muda radicalmente.
4a – Hemorragia intraplaca (HIP)
É o marcador mais consistente de risco futuro.
Sintomáticos
Mesmo com estenose moderada (50–69%): Forte argumento para CEA precoce.
Assintomáticos
Se:
- HIP documentada
- Progressão de estenose
- Expectativa de vida > 5 anos
Pode-se discutir revascularização individualizada.
Estudos mostram:
- HR até 11 para recorrência ipsilateral
HIP é provavelmente o maior modificador de risco independente da estenose.
4b – Ruptura de capa
Estado instável ativo.
Conduta:
- Sintomáticos → CEA urgente
- Assintomáticos com ruptura evidente → forte consideração para intervenção
A biologia da placa aqui se assemelha ao conceito de “placa vulnerável coronária”.
4c – Trombo intraluminal
Situação de altíssimo risco embólico.
Conduta:
- Anticoagulação inicial (dependendo do contexto)
- Avaliação urgente para revascularização
- Discussão multidisciplinar imediata
OR > 100 para AVC de origem carotídea. Aqui o risco supera quase qualquer limiar de estenose.
CEA vs Stent no Contexto do Plaque-RADS
A morfologia também pode influenciar a escolha do método:
Placa com:
- HIP extensa
- Ulceração complexa
- Trombo
CEA tende a ser preferível (menor manipulação intraluminal)
Stent pode fragmentar o material e aumentar o risco embólico.
Já placas calcificadas e fibrosas podem ser mais favoráveis ao CAS.
Assintomáticos: Onde o Plaque-RADS Pode Mudar Paradigma
Hoje, a maioria dos assintomáticos é tratada clinicamente. Com o Plaque-RADS, Assintomático + HIP = risco semelhante a sintomático e este achado pode justificar revascularização seletiva. Isso pode redefinir critérios futuros.
Impacto no Seguimento por Imagem
Placas RADS 3–4:
- Seguimento mais curto
- RM seriada pode monitorar HIP
- US com avaliação de JBA e microflow
Placas RADS 1–2:
- Intervalos mais longos
O Que Ainda Falta para que o Plaque-RADS seja totalmente utilizado?
O artigo é conceitual. Ainda não há trials randomizados guiados por Plaque-RADS e algoritmos terapêuticos formalmente validados com a classificação Plaque-RADS. Entretanto, o artigo prepara o terreno para: “revascularizar a biologia da placa, não apenas estenose.”
Síntese Prática para Decisão Clínica
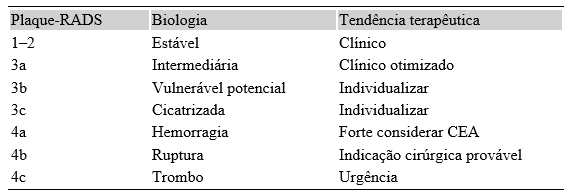
Conclusão Estratégica
O Plaque-RADS não substitui as diretrizes atuais, mas introduz a variável mais importante da doença carotídea: atividade biológica da placa.
Assim, ele pode evitar cirurgias desnecessárias em placas estáveis; pode indicar cirurgia em estenoses moderadas instáveis; refina decisão entre CEA e CAS; permite personalização terapêutica real.
E você? Já conhecia o plaque-RADS? Já utiliza na sua prática clínica? Acha que ele vai “pegar”? Eu já uso e adoro! Acho que vai pegar sim, mas precisamos validar essa classificação! Topa estudarmos isso?
