Aproximadamente 0.2-0.4% dos pacientes com prolapso da valva mitral (PVM) evoluem com morte súbita cardíaca a cada ano. Acredita-se que o fenótipo arrítmico do PVM seja responsável pela presença de arritmias ventriculares malignas com potencial para morte súbita (MS), cuja taxa anual é estimada em 0.14 eventos para cada 100 pacientes.
Alguns achados são considerados de risco para a síndrome arrítmica do PVM. São eles:
- Inversão de onda T nas derivações inferiores,;
- Documentação de extrassístoles ventriculares polimórficas frequentes no Holter;
- Prolapso de ambos os folhetos;
- Aumento do átrio esquerdo;
- Fração de ejeção (FE) do ventrículo esquerdo < 50%;
- Presença de realce tardio na ressonância magnética (RM) cardíaca;
- Disjunção do anel mitral (MAD);
- Insuficiência mitral importante;
Quando presente, a extensão da disjunção do anel posterior da valva mitral é um parâmetro relevante. Além disso, aumento da dispersão mecânica do ventrículo esquerdo (VE) e redução do strain global longitudinal (SGL) também são achados associados a um maior risco de arritmia ventricular em pacientes assintomáticos com MAD.
Assim sendo, a avaliação do PVM deve ser criteriosa a fim de se conseguir estabelecer, com assertividade, a presença ou não de fatores de risco anatômicos para a síndrome arrítmica.
Em 1986 um estudo sistemático conduzido por Hutchins et al., através de análise patológica de 900 corações de indivíduos adultos, descreveu o padrão anatômico de inserção do ânulo fibroso mitral junto à parede livre do ventrículo esquerdo e sua convergência com o átrio esquerdo (AE) – figuras A e B.
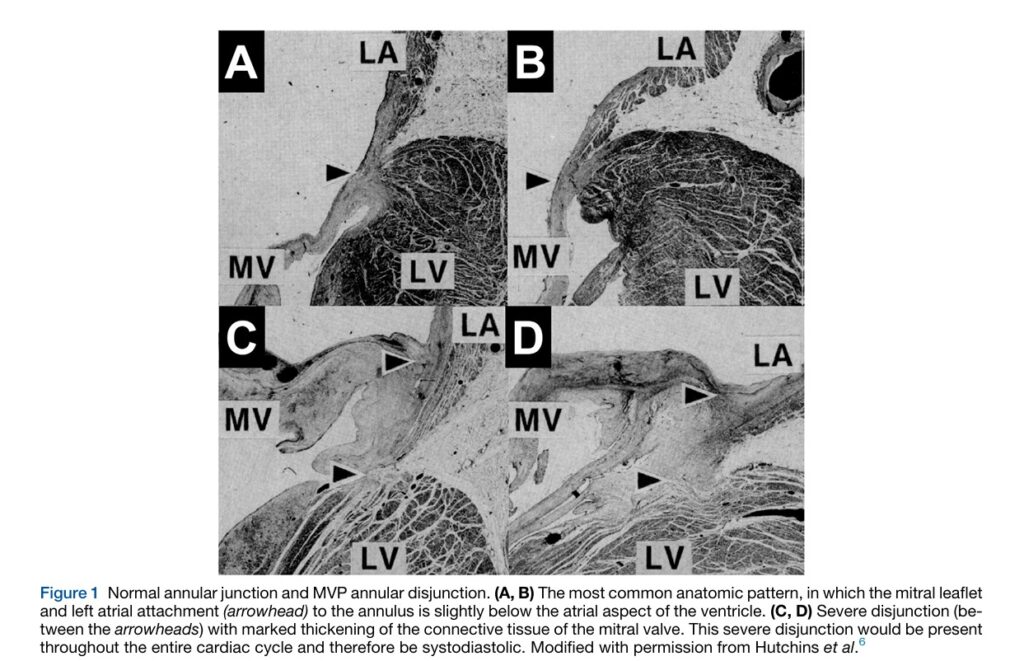
Na presença de MAD, o ponto de inserção do AE e da valva mitral no anel fibroso é deslocado posteriormente em relação à parede do VE, criando uma distância entre o VE e esse ponto de inserção, dando a aparência de que o folheto posterior da valva mitral se insere diretamente na parede do AE (figuras B e C).
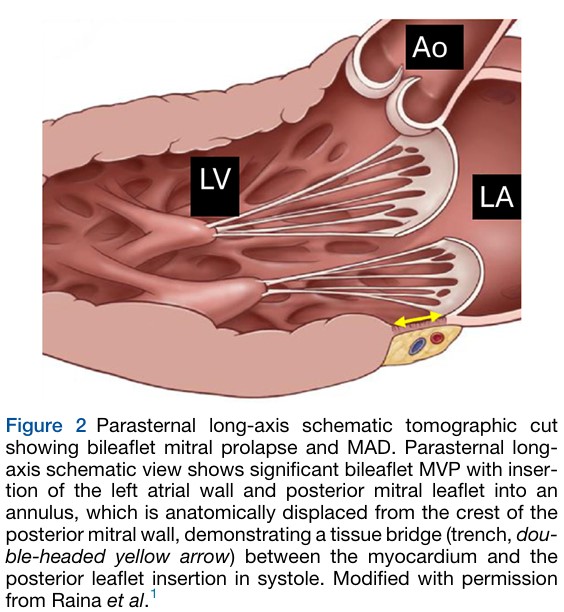
Esse deslocamento posterior do anel fibroso ocorre como uma variação anatômica permanente e, portanto, deve estar presente durante a sístole e a diástole (!!!).
E aí vem a complicação …
De acordo com o International Expert Consensus Statement de 2022 sobre MAD e síndrome arrítmica do PVM, a disjunção do anel mitral é um achado sistólico, caracterizado pela separação entre o miocárdio do VE e o anel valvar mitral na região que suporta o anel posterior, visualizada no eixo longo da janela paraesternal.
Esta descrição passa a impressão de que se trata de um processo dinâmico que ocorre durante a sístole, não havendo esta separação na diástole.
Contudo, esse mesmo documento recomenda que a avaliação seja realizada durante todo o ciclo cardíaco (sístole e diástole, portanto) ao mesmo tempo que fala em enfatizar a avaliação apenas na sístole (“frame by frame analysis from early to late systole”) para excluir a possibilidade de que o prolapso de tecido excessivo do folheto posterior, partindo de um anel valvar com implantação habitual, possa ficar justaposto à parede posterior do AE e apresentar uma falsa aparência de MAD – Figura B.
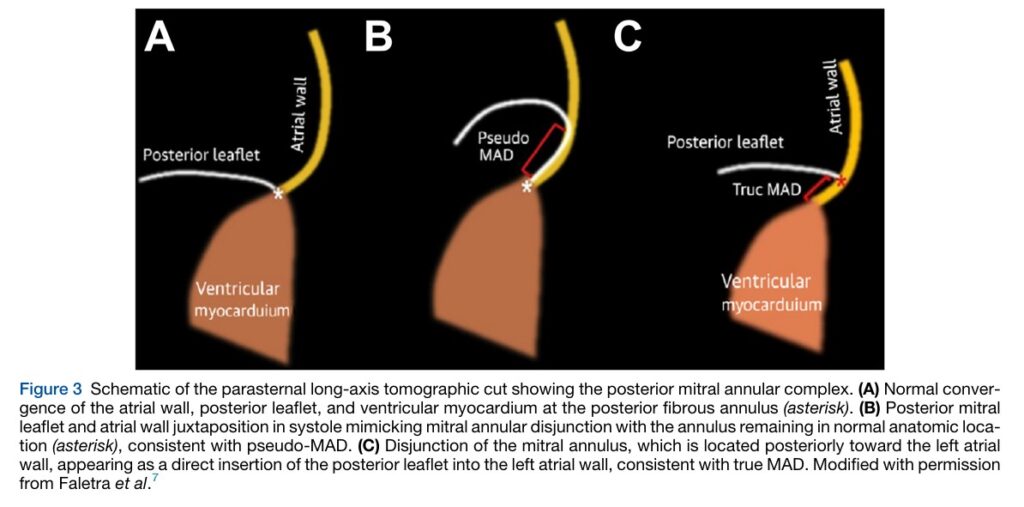
Teríamos, então, nesta situação o chamado pseudo MAD. O grande desafio agora é diferenciar esta condição que se assemelha à disjunção (mas não é) da MAD verdadeira.
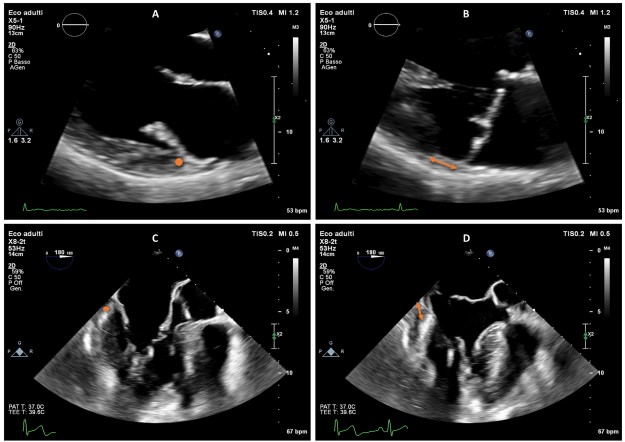
Faletra et al. propõe que a disjunção esteja sempre presente e, portanto, deve ser visualizada durante todo o ciclo cardíaco. Esta seria uma forma de diferenciar a MAD verdadeira do prolapso do folheto posterior cujo tecido se justapõe à parede posterior do átrio direito (como se fosse um tapete).
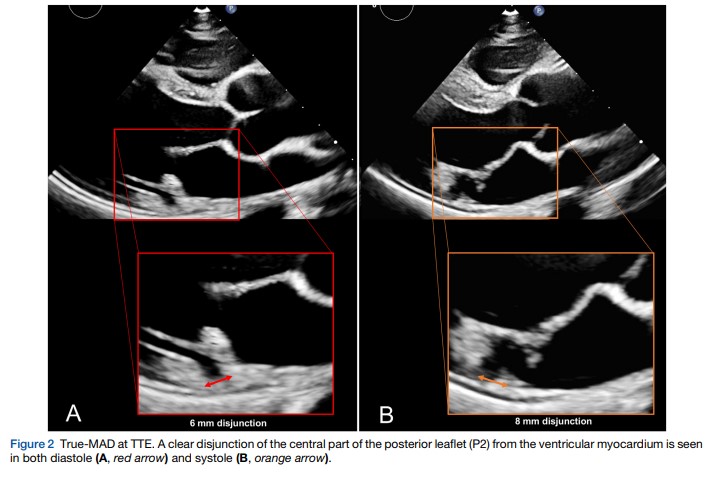
Em um estudo publicado no JASE (falaremos dele em breve …), Fiore et al. avaliou retrospectivamente 603 exames ecocardiográficos de pacientes com PVM mixomatoso e achou uma prevalência de 7% de MAD verdadeira, enquanto que a pseudo MAD foi documentada em 37% dos pacientes do estudo.
Neste mesmo estudo, quando considerado o “critério” de que a disjunção precisa estar presente tanto na sístole quanto na diástole, 84% dos diagnósticos de MAD foram reclassificados como pseudo MAD.
Outra característica importante é que a prevalência de pseudo MAD aumenta de acordo com a gravidade da insuficiência mitral em razão da piora do prolapso do folheto posterior, enquanto que a MAD verdadeira não sofre influência da magnitude da regurgitação valvar.
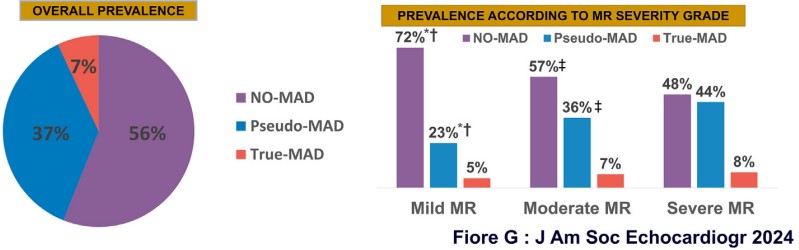
Vale ressaltar que, embora os resultados deste estudo sejam apenas descritivos, tanto os pacientes com MAD verdadeira e pseudo MAD exibiram maiores níveis de fibrose miocárdica, pela RM cardíaca, comparados com aqueles pacientes que apresentavam apenas PVM.
A MAD pode se apresentar de 05 diferentes formas no PVM:
(1) MAD sistodiastólica fixa – sem alongamento da distância;
(2) MAD sistodiastólica alongada – aumento da distância durante a sístole;
(3) MAD sistólica verdadeira – observada principalmente durante a sístole, mas presente na diástole;
(4) Pseudo MAD isolada;
(5) MAD verdadeira + pseudo MAD (aí você me quebra !!!) –
Graduado em medicina pela Universidade Potiguar (UnP). Possui residência em Clínica Médica pelo Hospital Universitário Onofre Lopes – HUOL (UFRN) e em Cardiologia pelo Procape – UPE. Porta o título de especialista em Cardiologia pela Sociedade Brasileira de Cardiologia (SBC) e é pós-graduado em Ecocardiografia, pela ECOPE.
Excelente, parabéns
Excelente artigo!! É um tema que sempre gera dúvidas.
Parabéns Caio !!
Seu texto está muito bom!