
E epidemiologia precisa da presença de cardiomiopatia hipertrófica (CMPH) associada a estenose valvar aórtica (EAo) não é bem documentada dada a raridade (relativa) da coexistência destas duas condições.
Porém, é esperado que, com os avanços da ecocardiografia e dos outros métodos diagnósticos na cardiologia, haja um reconhecimento mais frequente dessa associação. Dados americanos a partir da análise de 207.880 pacientes submetidos à troca valvar aórtica percutânea (TAVI), entre 2014 e 2018, indicam uma prevalência de 0.38% de CMPH obstrutiva associada a EAo.
Embora diretrizes atuais abordem o tema, a análise desses pacientes na vida real acaba sendo um verdadeiro desafio dada a complexidade e dificuldade técnica para estabelecer parâmetros confiáveis.
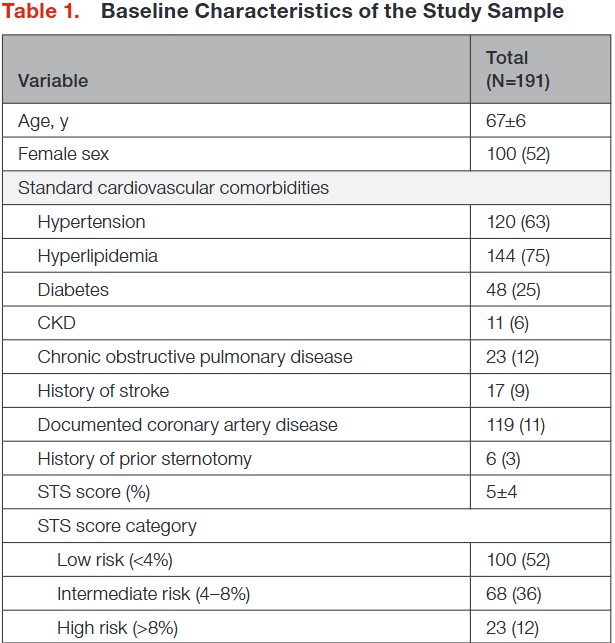
Um estudo publicado em 2021 identificou 191 pacientes com o fenótipo obstrutivo da CMPH e com EAo, que foram encaminhados para miomectomia e troca valvar aórtica durante um período de 16 anos.

Destes pacientes, todos foram submetidos ao estudo transesofágico, bem como a testes hemodinâmicos invasivos para se estabelecer a gravidade da disfunção valvar em razão dos desafios técnicos para aplicação de parâmetros convencionais, como equação de continuidade, diante da presença de uma fisiologia de “dupla obstrução”.
Caracteristicamente, esses pacientes tendem a ter idades mais avançadas quando comparados com pacientes portadores de CMPH obstrutiva isolada, sem haver predominância de sexo. Neste estudo citado, apesar de uma maior complexidade cirúrgica, a mortalidade intra-hospitalar dos pacientes submetidos à miomectomia com troca valvar aórtica foi baixa (1.5%), enquanto que o esperado, segundo o escore de risco da Sociedade de Cirurgiões Torácicos, seria uma taxa em torno de 5% de risco predito.
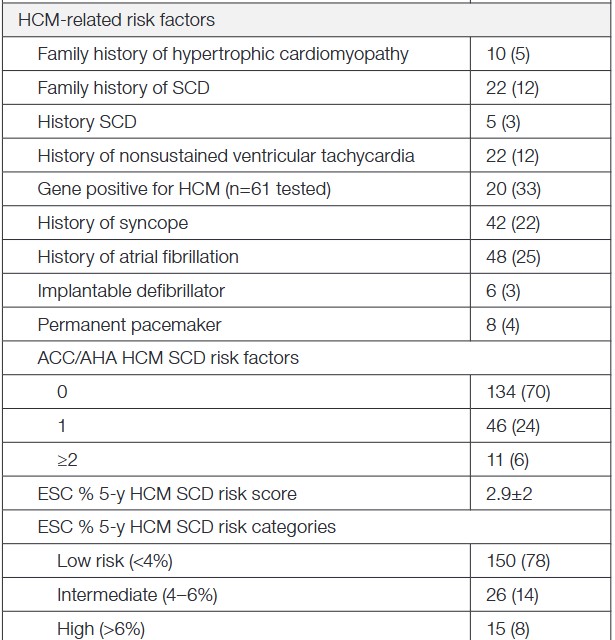
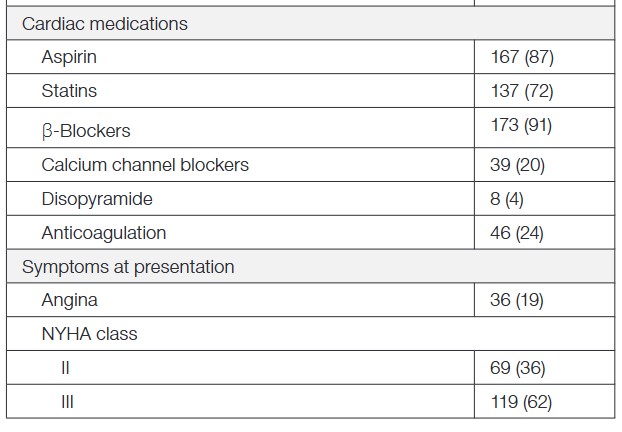
Aqui temos duas grandes questões: (1) dificuldade de assegurar que a hipertrofia miocárdica, nos casos em que ela apresente um perfil simétrico, seja geneticamente determinada, uma vez que a presença de EAo também leva ao aumento da espessura diastólica das paredes; e (2) definir a gravidade da disfunção valvar na presença de um padrão de “dupla obstrução”, ou seja, gradientes elevados na via de saída do ventrículo esquerdo (VE) e no fluxo transvalvar aórtico.

Por “sorte”, a maior parte dos casos relatados apresenta o fenótipo septal assimétrico de CMPH, eliminando o fator “1” de confusão diagnóstica, porém é importante lembrar de diagnósticos diferenciais como amioloidose cardíaca, doença de Danon, doença de Fabry e cardiomiopatia hipertensiva.
Quanto à avaliação ecocardiográfica da EAo, a análise a partir da equação de continuidade não deve ser utilizada para determinar a área valvar aórtica (já que a análise do fluxo da via de saída do VE estará comprometida pelo componente obstrutivo da CMPH). Parâmetros subjetivos como o grau de calcificação valvar e mobilidade dos folhetos podem ser cruciais neste contexto, muito embora a medida através da planimetria dificilmente será factível nos casos de EAo degenerativa uma vez que a presença de calcificação significativa (imagem B) irá gerar artefatos de reverberação e sombra acústica.
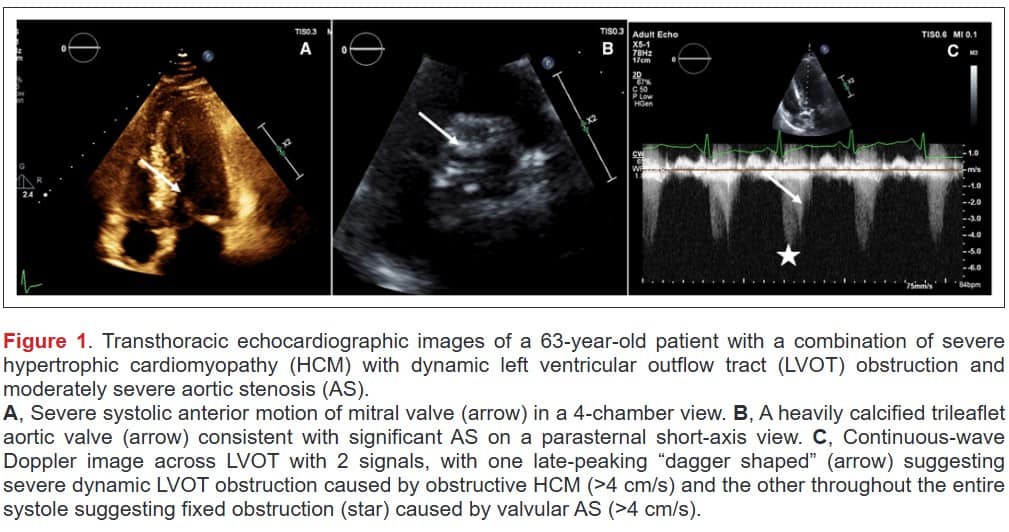
Outros métodos diagnósticos, portanto, devem ser utilizados, como por exemplo o escore de cálcio da valva aórtica através da tomografia computadorizada que, além de já ter se mostrado como uma variável com valor prognóstico, permite também a realização da planimetria para a estimativa da área valvar.
O padrão clássico da curva de Doppler relacionado ao fator obstrutivo da CMPH é descrito como em “formato de adaga”, com o pico sistólico ocorrendo de forma tardia durante a sístole.
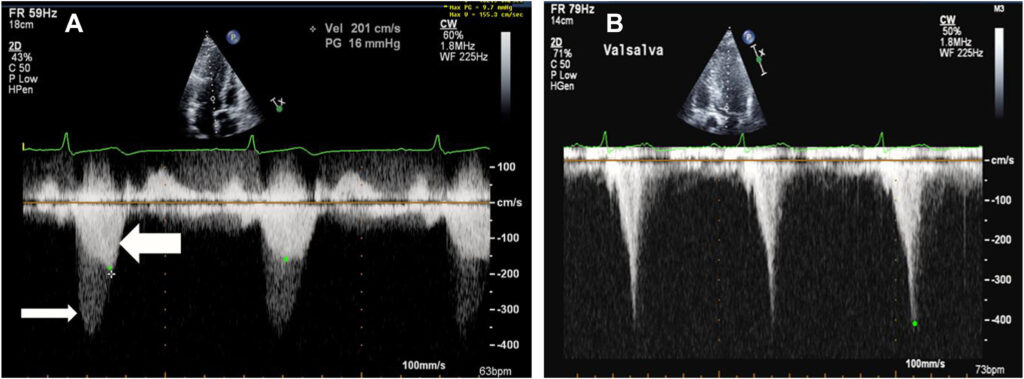
Esse padrão é distinto do aspecto em “parábola” observado na EAo, o qual apresenta o pico sistólico na proto ou mesossístole nos casos de estenose leve ou moderada, mas pode apresentar pico sistólico tardio na disfunção importante. A utilização do Doppler pulsátil pode auxiliar na diferenciação da origem da obstrução.
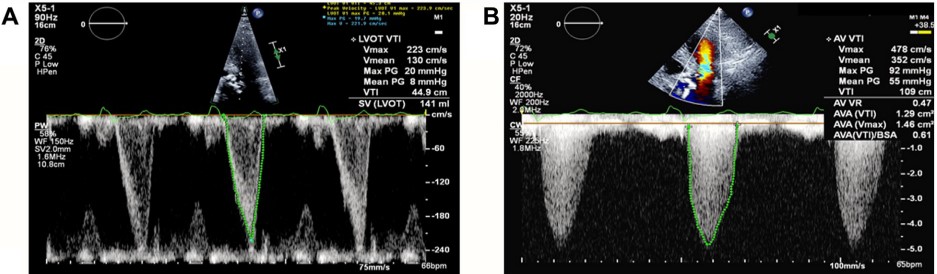
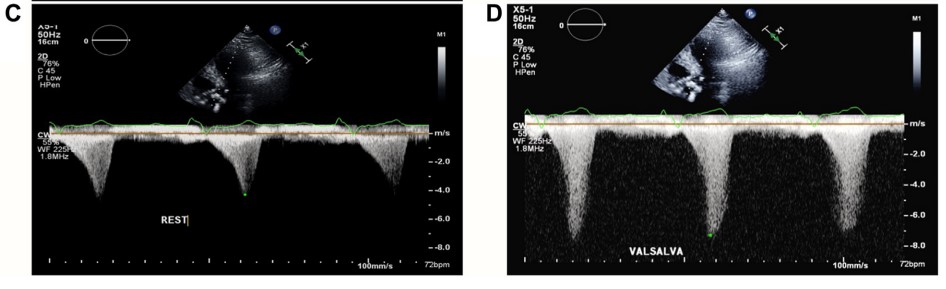
A curva do Doppler, ainda, pode sofrer influência e ficar “contaminada” quando na presença de insuficiência mitral (IMi) associada (em razão do movimento sistólico anterior do folheto anterior mitral). Esta curva de fluxo se inicia no começo da sístole e se intensifica durante a sístole final. Nesses casos, a velocidade máxima do fluxo mitral tende a ser maior que a do fluxo da EAo.
O não reconhecimento da obstrução subaórtica pode resultar em eventos pós cirúrgicos adversos. Embora o ecocardiograma transtorácico possa identificar a obstrução subaórtica e a diferenciar da EAo, a avaliação acurada da estenose aórtica se torna um desafio já que os conceitos utilizados para a equação de Bernoulli simplicada não são válidos neste contexto e podem superestimar o grau de estenose valvar.
Quando a velocidade proximal é > 1.5 m/s, por exemplo, a utilização da equação de Bernoulli não simplificada (P = 4V2² – V1², em que P é o gradiente pressórico, V1 é a velocidade proximal e V2, a velocidade distal à estenose) é recomendada. Embora o gradiente máximo possa ser calculado desta forma, o mesmo não se aplica para o gradiente médio (!!!). Desta maneira, a análise invasiva muitas vezes é necessária nos casos em que há dúvida quando à graduação da disfunção valvar.
A estimativa dos gradientes pressóricos em cada nível de obstrução é deveras importante, sobretudo quando pensamos na troca valvar transcateter, uma vez que o conhecimento do maior ponto de obstrução (VSVE x fluxo transvalvar) será determinante para a seleção de pacientes para os diferentes tipos de tratamento (miomectomia + troca valvar aórtica x TAVI + ablação alcoólica septal).
Portanto, a presença concomitante de EAo e CMPH obstrutiva é um cenário extremamente desafiador e que demanda auxílio de outras técnicas diagnósticas para uma avaliação confiável. Na próxima semana trarei alguns casos para exemplicar tamanha complexidade.
Graduado em medicina pela Universidade Potiguar (UnP). Possui residência em Clínica Médica pelo Hospital Universitário Onofre Lopes – HUOL (UFRN) e em Cardiologia pelo Procape – UPE. Porta o título de especialista em Cardiologia pela Sociedade Brasileira de Cardiologia (SBC) e é pós-graduado em Ecocardiografia, pela ECOPE.