Finalizando a série sobre o papel da dispersão mecânica (PSD) como parâmetro preditor de arritmias, trago agora um artigo que fala sobre o tema no contexto do prolapso da valva mitral (PVM).
Como sabemos, o PVM é condição com prevalência estimada em 2-3% da população geral. Destes, cerca de 0.8-2.5% irão apresentar parada cardíaca ou morte súbita cardíaca. Desta forma, é importante identificar variáveis que possam predizer o risco de desenvolvimento de arritmias ventriculares no sentido de identificar aqueles pacientes sob maior risco.

Estudo que avaliou 32 pacientes com síndrome arrítmica associada ao PVM, com histórico de ectopias ventriculares complexas no holter (n = 23) ou necessidade de implante de cardiodesfibrilador implantável – CDI (n = 9), sendo comparados com outros 27 pacientes portadores de PVM sem evento arrítmico, bem como 39 pacientes do grupo controle.
Arritmia ventricular complexa foi definida como (1) extrassístoles pareadas, (2) bigeminismo ventricular, (3) taquicardia ventricular não sustentada – TVNS ou (4) taquicardia ventricular sustenada – TV.
Pacientes com doença arterial coronária (DAC), infarto prévio, passado de cirurgia cardíaca, doença congênita cardíaca ou doença valvar aórtica significativa foram excluídos.
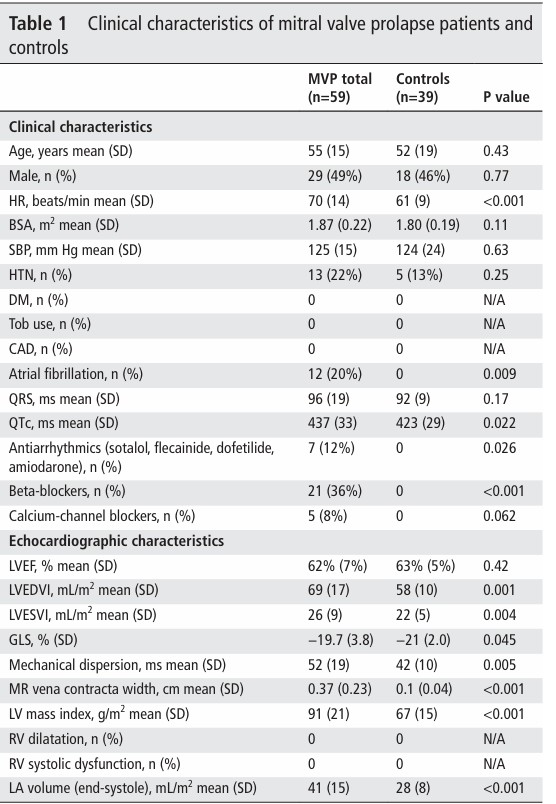
Os pacientes com PVM apresentaram maiores médias de frequência cardíaca (p < 0.001), intervalo QTc mais prolongados (p = 0.022) e maior taxa de utilização de medicações antiarrítmicas (p = 0.026).
Quando comparado com o grupo controle, os pacientes com PVM também apresentaram índices de volume diastólico e sistólico final maiores, bem como maiores índices de massa, volume indexado do átrio esquerdo (AE) e regurgitação mitral mais significativa (p < 0.05).
A maior parte dos pacientes tinha prolapso de ambos os folhetos mitral (56%) e regurgitação valvar de grau leve, com vena contracta < 0,30 cm (66%). Apenas 13 pacientes tinham disjunção do anel posterior (22%), sendo todos eles associado a prolapso de ambos os folhetos.
O strain global longitudinal (SGL) do ventrículo esquerdo (VE) foi, de forma geral, menor entre os pacientes com PVM (19.7% x 21%, p = 0.045). Da mesma forma, aqueles com PVM apresentaram maiores valores de dispersão mecânica (52 ms x 42 ms, p – 0.005) em comparação com o grupo controle.
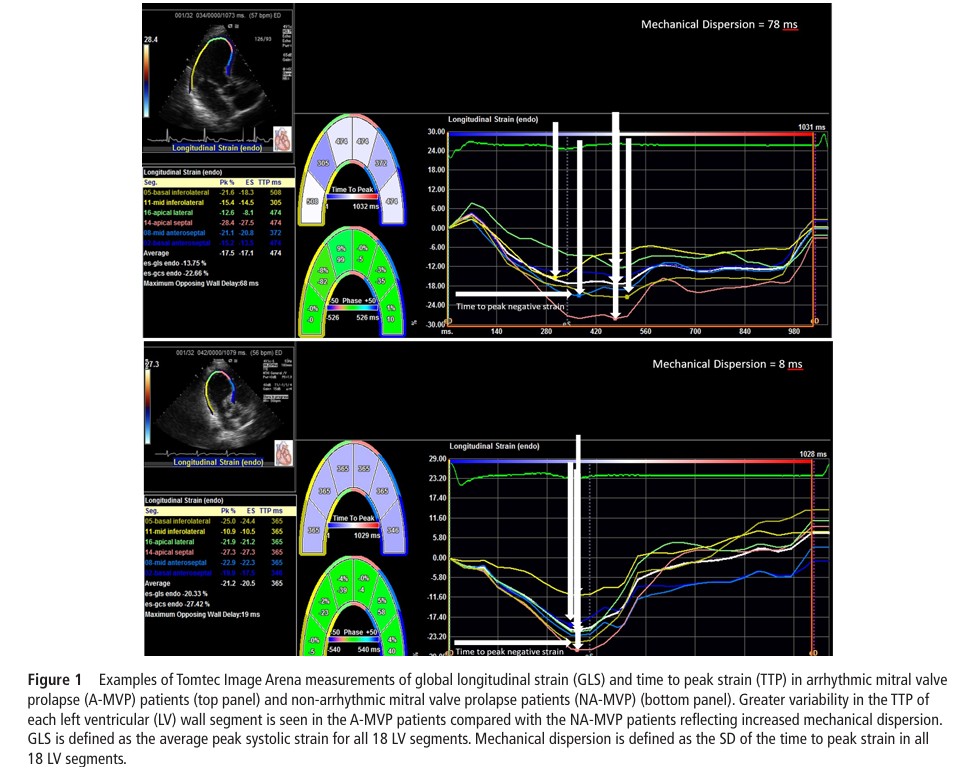
Do total de 59 pacientes com PVM, 32 tinham a forma arrítmica. Desses, 23 apresentaram ectopia ventricular complexa, sendo 17 com taquicardia ventricular, ao Holter. 09 pacientes tiveram necessidade de implante de CDI para prevenção secundária.
Quando comparado os pacientes portadores de PVM com e sem eventos arrítmicos, , não foram observadas diferenças nos parâmetros clínicos, com exceção do maior uso de medicações antiarrítmicas entre aqueles pacientes com histórico de arritmia (p = 0.009).
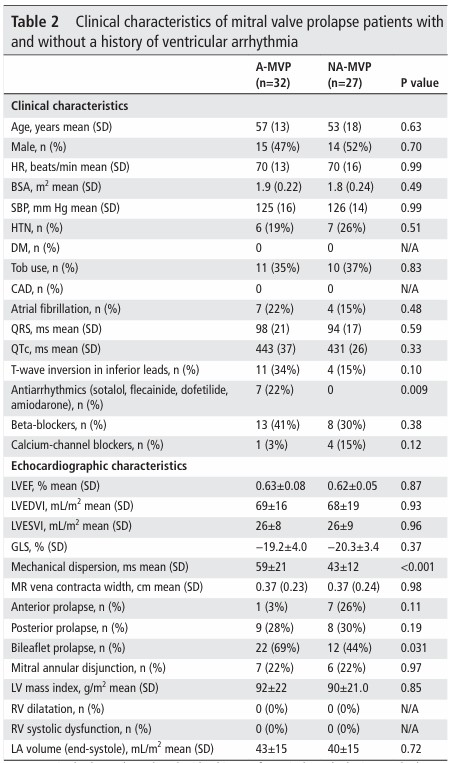
Da mesma forma, não houve diferenças em relação aos parâmetros ecocardiográficos convencionais, com exceção de uma maior incidência de prolapso de ambos os folhetos no grupo da síndrome arrítmica (p = 0.031).
A quantidade de pacientes com insuficiência mitral moderada ou importante, ou com disjunção do anel posterior foi similar entre os dois grupos (p = 0.56 e p = 0.97, respectivamente).
O SGL também foi semelhante entre eles (p = 0.37). Já a dispersão mecânica, por sua vez, foi significativamente maior nos pacientes com PVM e arritmias ventriculares (média 59 ± 21 ms x 43 ± 12 ms, p < 0.001).
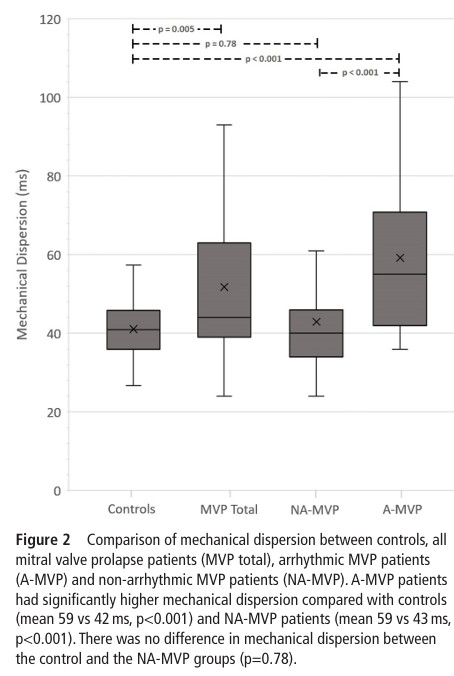
Dentro do grupo com eventos arrítmicos, aqueles portadores de CDI apresentaram os maiores valores de dispersão mecânica comparados com aqueles com documentação de ectopia ventricular complexa (67 ± 17 ms x 56 ± 22 ms, p = 0.078).
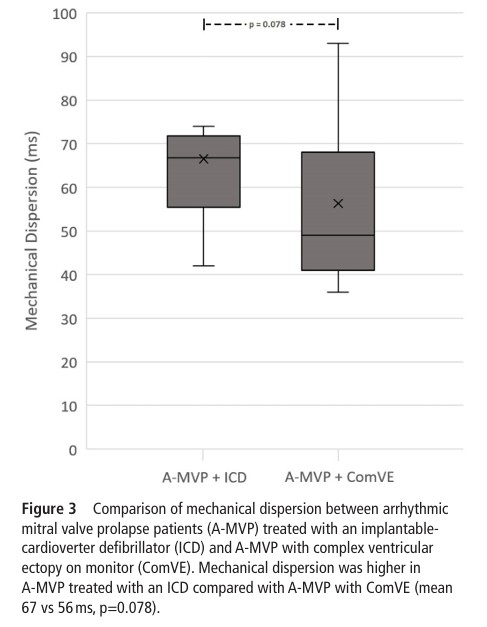
A dispersão mecânica, contudo, não apresentou diferença significativa entre aqueles pacientes com PVM de apenas um dos folhetos ou de ambos (média 48 ± 16 ms x 55 ± 21 ms, p = 0.33).
Quando comparado com o grupo controle, aqueles pacientes com PVM sem arritmia ventricular apresentaram valores de PSD similares (médio 43 ± 12 ms x 42 ± 19 ms, p = 0.78).
Em modelo de multivariáveis incluindo dispersão mecânica, prolapso de ambos os folhetos e diâmetro da vena contracta, apenas a dispersão mecânica se mostrou como variável preditora, de forma significativa, do risco de arritmias (OR 1.1, 95%IC: 1.02-1.11, p = 0.006).
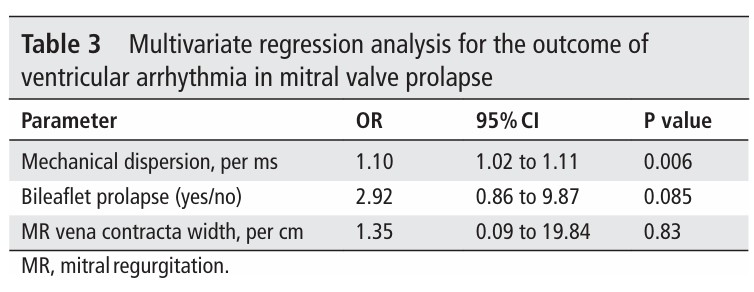
Em um segundo modelo incluindo apenas a dispersão mecânica e o diâmetro da vena contracta, o PSD continuou como único preditor significativo (OR 1.1, 95%IC: 1.02-1.12, p = 0.004).
O prolapso de ambos os folhetos foi o preditor mais importante no modelo incluindo apenas o envolvimento dos folhetos anterior e posterior, e o diâmetro da vena contracta (OR 3.6, 95%IC: 1.2-10.8, p = 0.023).
Portanto, o aumento da dispersão mecânica pode ajudar a identificar aqueles pacientes portadores de PVM e com maior risco de desenvolver eventos arrítmicos, sendo uma variável independente da função ventricular esquerda, grau da regurgitação mitral e o tipo de envolvimento dos folhetos valvares.
Um outro estudo publicado na European Heart Journal – Cardiovascular Imaging, com 63 pacientes portadores de PVM (37 mulheres e 29 homens) e com queixa de palpitação também avaliou o papel da dispersão mecânica para predizer arritmias ventriculares.

A documentação de alguma arritmia ventricular foi observada em 32 dos 63 pacientes, sendo o bigeminismo ventricular o tipo mais comum. Diferentemente dos parâmetros ecocardiográficos convencionais, a dispersão mecânica e a disjunção do anel mitral foram significativamente maiores no grupo de pacientes com arritmia ventricular (P<0.001).
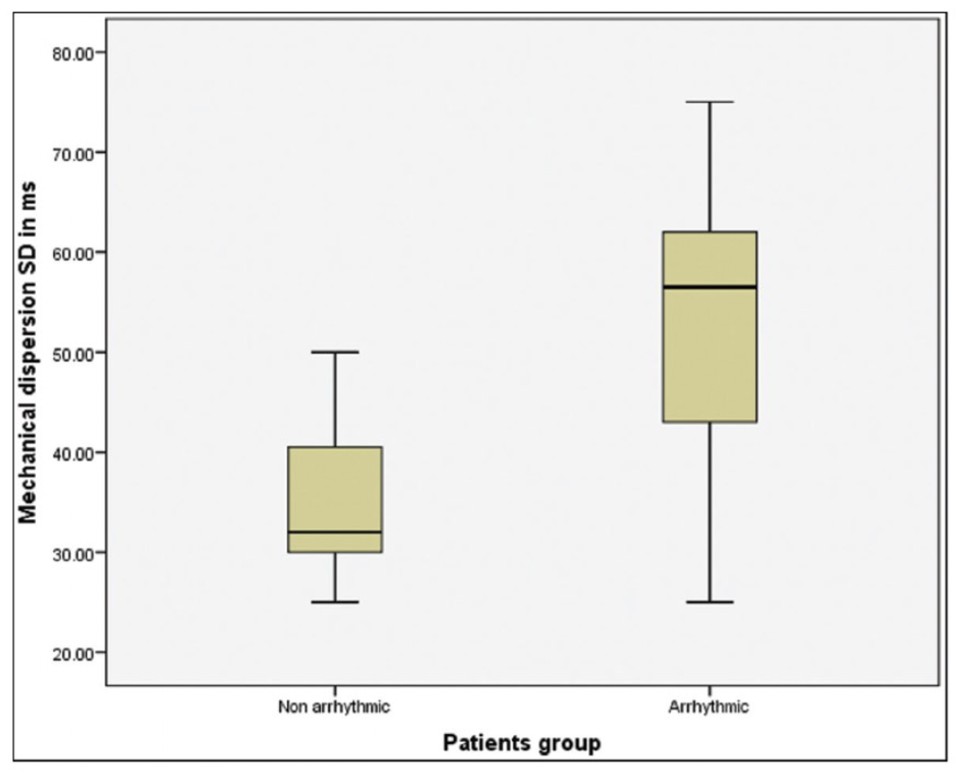
Ainda, a dispersão mecânica foi maior entre aqueles com ectopias ventriculares frequentes quando comparados com aqueles com ectopias ventriculares não frequentes (P = 0.003). O ponto de corte da dispersão mecânica para predizer arritmia foi de 35.1 ms ou mais, com sensibilidade de 87% e especificidade de 71%. Já para a disjunção do anel mitral, o valor considerado foi de 2.7 mm ou mais (sensibilidade 82% e especificidade de 60%).
Graduado em medicina pela Universidade Potiguar (UnP). Possui residência em Clínica Médica pelo Hospital Universitário Onofre Lopes – HUOL (UFRN) e em Cardiologia pelo Procape – UPE. Porta o título de especialista em Cardiologia pela Sociedade Brasileira de Cardiologia (SBC) e é pós-graduado em Ecocardiografia, pela ECOPE.