Recentemente tivemos a publicação da Revista Norte Nordeste de Cardiologia com foco nas cardiopatias raras.

Nesta edição, Prof. Castillo, nosso diretor acadêmico e maior referência (seja na ecocardiografia ou no quesito humildade) escreveu sobre o uso do Strain na diferenciação das cardiopatias raras.

Vamos fazer uma série de postagens resumindo esta revisão com conteúdo atualizado e completo sobre o uso dessa técnica no contexto de doenças raras e, quase sempre, desafiadoras.
#CARDIOMIOPATIAS HIPERTRÓFICAS DE CAUSA GENÉTICA:
As cardiomiopatias hipertróficas (CMH) correspondem à maioria das doenças raras, existindo fenótipos distintos. De forma geral, caracterizam-se pela presença de desarranjo miofibrilar e aumento da fibrose intersticial.
1-Hipertrofia Septal Assimétrica Obstrutiva: este fenótipo apresenta deslocamento anterior dos músculos papilares, o que provoca alongamento e anteriorização do aparelho valvar mitral, que se aproxima do septo interventricular hipertrofiado, favorecendo a ocorrência de movimento anterior sistólico, cujo mecanismo principal é a sucção provada pelo aumento da velocidade de fluxo na via de saída do ventrículo esquerdo (VSVE) – efeito Venturi.
Esta obstrução é progressiva, sendo maior no final da sístole, resultando em um traçado de Doppler espectral com velocidade aumentada e pico tardio.
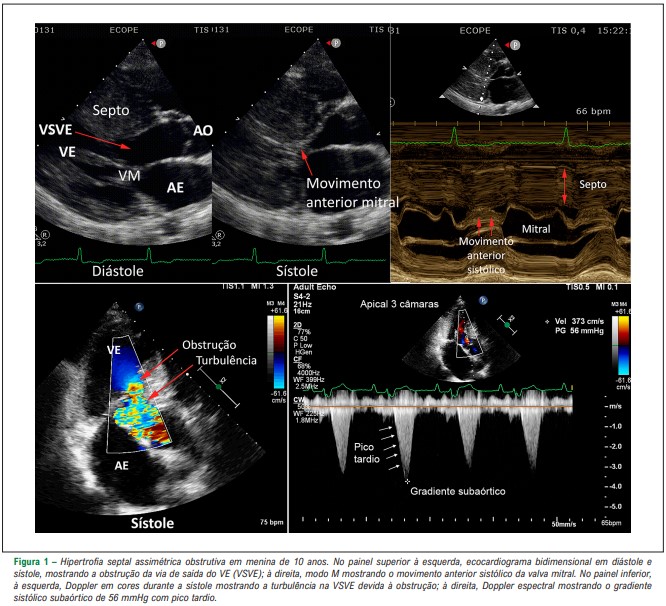
O deslocamento anterior mitral (SAM) também provoca deslizamento (tethering) dos folhetos da valva com ocorrência de refluxo. O átrio esquerdo (AE), em geral, está dilatada , em parte pelo refluxo mitral, assim como pela alteração da função diastólica.
Do ponto de vida ecocardiográfico, considera-se hipertrofia septal assimétrica o aumento da espessura diastólica septal ≥ 15 mm com relação septo/aprede > 1,3. A obstrução subaórtica, por sua vez, é considerada significativa quando o gradiente sistólico é ≥ 30 mmHg.
Neste tipo de hipertrofia localizada, a avaliação do strain miocárdico apresenta diminuição segmentar nas áreas com maior desarranjo miofibrilar, quando ainda não há alteração da função sistólica (estágio I, subclínico) e diminuição global, indicando o grau de disfunção sistólica, quando a CMH é mais significativa (estágio II com remodelamento ventricular), com maior diminuição segmentar.
Em pacientes em estágio III, com alterações mais importante, inclusive com dilatação do ventrículo esquerdo (VE), a diminuição do strain longitudinal é mais significativa, muitas vezes mascarando as alterações segmentares.
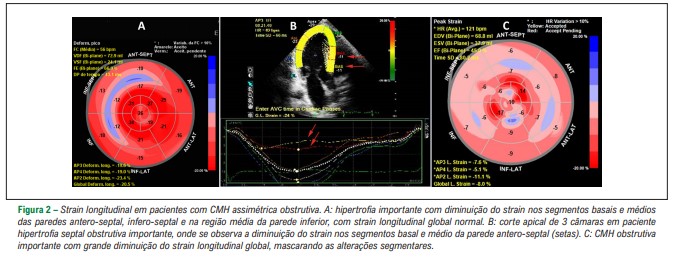
2-Hipertrofia Septal Assimétrica Não Obstrutiva: esta forma apresenta desarranjo miofibrilar semelhante à forma obstrutiva, porém com menor ou nenhum deslocamento anterior dos músculos papilares e do aparelho subvalvar, pelo que não se detecta obstrução dinâmica da VSVE em repouso ou durante o exercício ou com provas provocativas.
A hipertrofia apical caracteriza-se pelo acometimento dos segmentos apicais, apresentando o aspecto de “as de espadas” no final da sístole, podendo haver gradiente intraventricular decorrente da obliteração apical. O strain miocárdico mostra, geralmente, diminuição nos segmentos apicais. Em alguns casos, entretanto, esta alteração não é tal evidente.

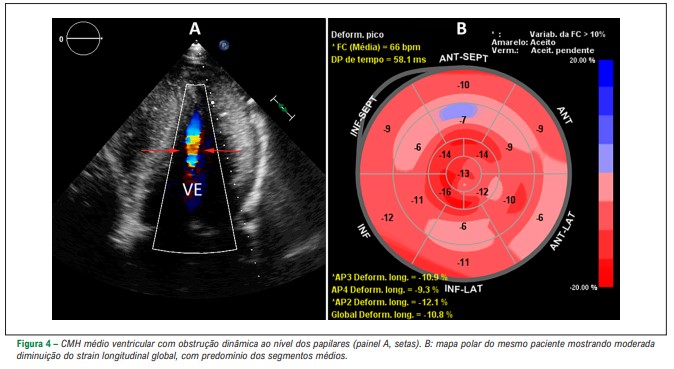
A hipertrofia médio ventricular é o fenótipo menos frequente e consiste na hipertrofia ao nível dos músculos papilares e na parede lateral do VE. Não provoca obstrução dinâmica ao nível da VSVE, mas frequentemente ocorre gradiente médio-ventricular, algumas vezes com dilatação aneurismática apical. Conforme o grau de desarranjo miofibrilar e da infiltração por fibrose, o strain longitudinal do VE pode ser normal ou diminuído, mas com maior comprometimento na região mais hipertrófica.
A hipertrofia generalizada (simétrica) apresenta espessura > 15 mm na maioria dos segmentos, sem evidências de outras causas que a justifique. Sua prevalência é estimada em 10% dos casos de CMH e sua origem genética é comprovada em 30-40% dos pacientes. Devido à intensa hipertrofia, com frequência provoca obstrução dinâmica, porém sem obstrução ao nível da VSVE, semelhante à observada na forma médio-ventricular.
O strain longitudinal do VE apresenta diversos graus de diminuição, de acordo com o acometimento miofibrilar, com diminuição difusa do strain segmentar.
Em número menor de casos pode ser observada hipertrofia localizada de outras paredes, como lateral ou inferior, comportando-se de forma semelhante às hipertrofias assimétricas não obstrutivas, com alterações difusas do strain longitudinal com maior diminuição nas regiões mais hipertróficas.
3-Hipertrofia isolada dos músculos papilares: ainda em investigação sobre sua origem genética, a hipertrofia isolada dos músculos papilares com espessura miocárdica normal pode provocar angina, arritmias e até morte súbita. Caracteriza-se pelo diâmetro dos músculos papilares maior que 11 mm, medido no final da diástole.
Alterações do strain longitudinal não costumam ser observadas quando não há hipertrofia ventricular associada.
Ademais do strain longitudinal, a avaliação do strain circunferencial e da rotação miocárdica podem ser úteis na avaliação destas cardiopatias.
O strain circunferencial, por ser mais representativo das camadas mais externas do miocárdio (menos suscetíveis à disfunção do que a camada subendocárdica), em geral se altera mais tardiamente, acompanhando a diminuição dos parâmetros obtidos com o ecocardiograma convencional, como a fração de ejeção.
Sua diminuição, portanto, indica maior comprometimento da função sistólica ventricular.
A aferição do strain rate da onde e´, por sua vez, tem se firmado como um preditor de todos os graus de disfunção diastólica, pois avalia a eficiência do enchimento ventricular. Valores inferiores a 1,0 s se correlacionam com disfunção diastólica ventricular com sensibilidade de 84% e especificidade maior que 90%.
A rotação apical e o twisting são o resultado da conformação helicoidal do miocárdio que, com fibras subendocárdicas e subepicárdicas cruzadas quase em ângulo reto e tracionando as camadas em direções opostas, provocam rotação em sentido horário na região basal do VE e anti-horário na região apical.
Nas CMH a rotação apical e o twisting encontram-se aumentados, em parte para compensar a diminuição da deformação das camadas subendocárdicas, avaliadas pelo strain longitudinal. Sua diminuição indica maior comprometimento miocárdico, com fração de ejeção diminuída em grau importante.
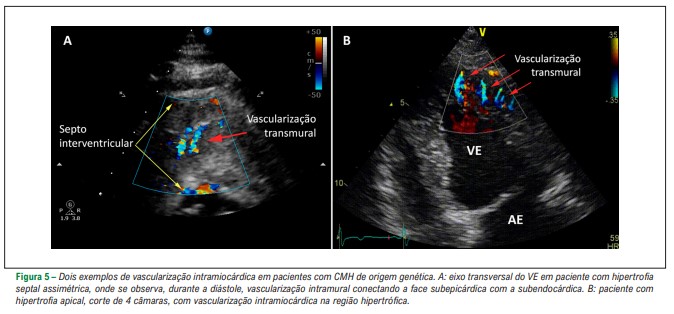
Outro parâmetro que pode ser avaliado no contexto das CMH é a alteração do fluxo intramural. Nas CMH de origem genética é frequente observar o aumento da vascularização miocárdica nas regiões mais afetadas, com vasos dilatados apresentando hiperfluxo, comunicando a camada subepicárdica com o subendocárdio.
Esta vascularização é atribuída à abertura de vasos colaterais, não visíveis em condições normais, destinados a aumentar o fluxo nas regiões mais hipertróficas. Esta vascularização não tem sido observadas em hipertrofias miocárdicas de outras etiologias.
Graduado em medicina pela Universidade Potiguar (UnP). Possui residência em Clínica Médica pelo Hospital Universitário Onofre Lopes – HUOL (UFRN) e em Cardiologia pelo Procape – UPE. Porta o título de especialista em Cardiologia pela Sociedade Brasileira de Cardiologia (SBC) e é pós-graduado em Ecocardiografia, pela ECOPE.